| Acide aminé: Les acides aminés sont des composés organiques qui contiennent des groupes fonctionnels amino (-NH 2 ) et carboxyle (-COOH), ainsi qu'une chaîne latérale (groupe R) spécifique à chaque acide aminé. Les éléments clés d'un acide aminé sont le carbone (C), l'hydrogène (H), l'oxygène (O) et l'azote (N), bien que d'autres éléments se trouvent dans les chaînes latérales de certains acides aminés. Environ 500 acides aminés naturels sont connus en 1983 (bien que seulement 20 apparaissent dans le code génétique) et peuvent être classés de plusieurs manières. Ils peuvent être classés selon les emplacements des groupes fonctionnels structurels de base en acides aminés alpha- (α-) , bêta- (β-) , gamma- (γ-) ou delta- (δ-) ; d'autres catégories concernent la polarité, le niveau de pH et le type de groupe de chaînes latérales (aliphatique, acyclique, aromatique, contenant de l'hydroxyle ou du soufre, etc.). Sous forme de protéines, les résidus d'acides aminés forment le deuxième composant en importance (l'eau est le plus important) des muscles et autres tissus humains. Au-delà de leur rôle de résidus dans les protéines, les acides aminés participent à un certain nombre de processus tels que le transport et la biosynthèse des neurotransmetteurs. |  |
| Acide aminé à chaîne ramifiée : Un acide aminé à chaîne ramifiée ( BCAA ) est un acide aminé ayant une chaîne latérale aliphatique avec une ramification. Parmi les acides aminés protéinogènes, il existe trois BCAA : la leucine, l'isoleucine et la valine. Les BCAA non protéinogènes comprennent l'acide 2-aminoisobutyrique. | 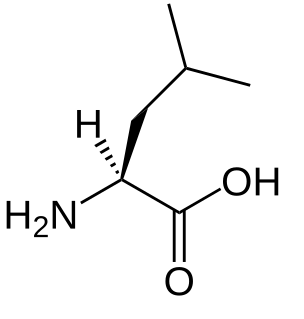 |
| Acide aminé essentiel : Un acide aminé essentiel , ou acide aminé indispensable , est un acide aminé qui ne peut pas être synthétisé de toutes pièces par l'organisme assez rapidement pour répondre à sa demande, et doit donc provenir de l'alimentation. Sur les 21 acides aminés communs à toutes les formes de vie, les neuf acides aminés que les humains ne peuvent pas synthétiser sont la phénylalanine, la valine, la thréonine, le tryptophane, la méthionine, la leucine, l'isoleucine, la lysine et l'histidine. | |
| Acide aminé: Les acides aminés sont des composés organiques qui contiennent des groupes fonctionnels amino (-NH 2 ) et carboxyle (-COOH), ainsi qu'une chaîne latérale (groupe R) spécifique à chaque acide aminé. Les éléments clés d'un acide aminé sont le carbone (C), l'hydrogène (H), l'oxygène (O) et l'azote (N), bien que d'autres éléments se trouvent dans les chaînes latérales de certains acides aminés. Environ 500 acides aminés naturels sont connus en 1983 (bien que seulement 20 apparaissent dans le code génétique) et peuvent être classés de plusieurs manières. Ils peuvent être classés selon les emplacements des groupes fonctionnels structurels de base en acides aminés alpha- (α-) , bêta- (β-) , gamma- (γ-) ou delta- (δ-) ; d'autres catégories concernent la polarité, le niveau de pH et le type de groupe de chaînes latérales (aliphatique, acyclique, aromatique, contenant de l'hydroxyle ou du soufre, etc.). Sous forme de protéines, les résidus d'acides aminés forment le deuxième composant en importance (l'eau est le plus important) des muscles et autres tissus humains. Au-delà de leur rôle de résidus dans les protéines, les acides aminés participent à un certain nombre de processus tels que le transport et la biosynthèse des neurotransmetteurs. |  |
| Azote assimilable par levure : L'azote assimilable de levure ou YAN est la combinaison d'azote aminé libre (FAN), d'ammoniac (NH 3 ) et d'ammonium (NH 4 + ) qui est disponible pour la levure de vin Saccharomyces cerevisiae à utiliser pendant la fermentation. En dehors des sucres fermentescibles glucose et fructose, l'azote est le nutriment le plus important nécessaire pour mener à bien une fermentation réussie qui ne se termine pas avant le point de sécheresse prévu ou voit le développement d'odeurs désagréables et de défauts de vin associés. Dans cette mesure, les viticulteurs complèteront souvent les ressources de YAN disponibles avec des additifs azotés tels que le phosphate diammonique (DAP). |  |
| Azote assimilable par levure : L'azote assimilable de levure ou YAN est la combinaison d'azote aminé libre (FAN), d'ammoniac (NH 3 ) et d'ammonium (NH 4 + ) qui est disponible pour la levure de vin Saccharomyces cerevisiae à utiliser pendant la fermentation. En dehors des sucres fermentescibles glucose et fructose, l'azote est le nutriment le plus important nécessaire pour mener à bien une fermentation réussie qui ne se termine pas avant le point de sécheresse prévu ou voit le développement d'odeurs désagréables et de défauts de vin associés. Dans cette mesure, les viticulteurs complèteront souvent les ressources de YAN disponibles avec des additifs azotés tels que le phosphate diammonique (DAP). |  |
| Aminoacyl ARNt synthétase : Une aminoacyl-ARNt synthétase , également appelée ARNt-ligase, est une enzyme qui fixe l'acide aminé approprié sur son ARNt correspondant. Il le fait en catalysant la transestérification d'un acide aminé apparenté spécifique ou de son précurseur à l'un de tous ses ARNt apparentés compatibles pour former un aminoacyl-ARNt. Chez l'homme, les 20 types différents d'aa-ARNt sont fabriqués par les 20 différentes aminoacyl-ARNt synthétases, une pour chaque acide aminé du code génétique. | 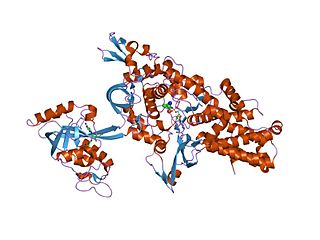 |
| Aminoacyl ARNt synthétase : Une aminoacyl-ARNt synthétase , également appelée ARNt-ligase, est une enzyme qui fixe l'acide aminé approprié sur son ARNt correspondant. Il le fait en catalysant la transestérification d'un acide aminé apparenté spécifique ou de son précurseur à l'un de tous ses ARNt apparentés compatibles pour former un aminoacyl-ARNt. Chez l'homme, les 20 types différents d'aa-ARNt sont fabriqués par les 20 différentes aminoacyl-ARNt synthétases, une pour chaque acide aminé du code génétique. |  |
| Alcanolamine : Les alcanolamines sont des composés chimiques qui contiennent à la fois des groupes fonctionnels hydroxyle (-OH) et amino (-NH 2 , -NHR et -NR 2 ) sur un squelette alcane. Le terme alcanolamine est un terme de classe large qui est parfois utilisé comme sous-classification. | |
| Alcanolamine : Les alcanolamines sont des composés chimiques qui contiennent à la fois des groupes fonctionnels hydroxyle (-OH) et amino (-NH 2 , -NHR et -NR 2 ) sur un squelette alcane. Le terme alcanolamine est un terme de classe large qui est parfois utilisé comme sous-classification. | |
| Aniline: L'aniline est un composé organique de formule C 6 H 5 NH 2 . Constituée d'un groupe phényle attaché à un groupe amino, l'aniline est l'amine aromatique la plus simple. C'est un produit chimique de base d'importance industrielle, ainsi qu'un matériau de départ polyvalent pour la synthèse chimique fine. Son utilisation principale est la fabrication de précurseurs de polyuréthane, de colorants et d'autres produits chimiques industriels. Comme la plupart des amines volatiles, elle a une odeur de poisson pourri. Il s'enflamme facilement, brûlant d'une flamme fumée caractéristique des composés aromatiques. |  |
| Liaison peptidique: Une liaison peptidique est un type amide de liaison chimique covalente reliant deux acides alpha-aminés consécutifs de C1 d'un acide alpha-aminé et N2 d'un autre, le long d'une chaîne peptidique ou protéique. |  |
| Acide aminocaproïque : L'acide aminocaproïque est un dérivé et un analogue de l'acide aminé lysine, ce qui en fait un inhibiteur efficace des enzymes qui se lient à ce résidu particulier. De telles enzymes comprennent des enzymes protéolytiques comme la plasmine, l'enzyme responsable de la fibrinolyse. Pour cette raison, il est efficace dans le traitement de certains troubles de la coagulation et il est vendu sous le nom de marque Amicar . L'acide aminocaproïque est également un intermédiaire dans la polymérisation du Nylon-6, où il est formé par hydrolyse par ouverture de cycle du caprolactame. La détermination de la structure cristalline a montré que l'acide 6-aminohexanoïque est présent sous forme de sel, au moins à l'état solide. |  |
| Esters aminés : Les esters aminés sont une classe d'anesthésiques locaux. Ils sont nommés pour leur liaison ester. | |
| Amine: En chimie organique, les amines (, UK également ) sont des composés et des groupes fonctionnels qui contiennent un atome d'azote basique avec une seule paire. Les amines sont formellement des dérivés de l'ammoniac, dans lesquels un ou plusieurs atomes d'hydrogène ont été remplacés par un substituant tel qu'un groupe alkyle ou aryle (ceux-ci peuvent être respectivement appelés alkylamines et arylamines ; les amines dans lesquelles les deux types de substituants sont liés à un atome d'azote peuvent être appelés alkylarylamines). Les amines importantes comprennent les acides aminés, les amines biogènes, la triméthylamine et l'aniline ; voir Category:Amines pour une liste d'amines. Les dérivés inorganiques de l'ammoniac sont également appelés amines, comme la monochloramine (NClH 2 ). | |
| Aminoglycoside : Les aminosides sont une catégorie médicinale et bactériologique de médicaments antibactériens à Gram négatif traditionnels qui inhibent la synthèse des protéines et contiennent comme partie de la molécule un glycoside amino-modifié (sucre). Le terme peut également désigner plus généralement toute molécule organique contenant des sous-structures de sucres aminés. Les antibiotiques aminosides présentent une activité bactéricide contre les aérobies Gram-négatifs et certains bacilles anaérobies où la résistance n'est pas encore apparue, mais généralement pas contre les bactéries Gram-positives et anaérobies Gram-négatives. | 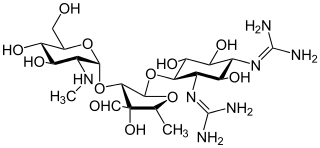 |
| Amine: En chimie organique, les amines (, UK également ) sont des composés et des groupes fonctionnels qui contiennent un atome d'azote basique avec une seule paire. Les amines sont formellement des dérivés de l'ammoniac, dans lesquels un ou plusieurs atomes d'hydrogène ont été remplacés par un substituant tel qu'un groupe alkyle ou aryle (ceux-ci peuvent être respectivement appelés alkylamines et arylamines ; les amines dans lesquelles les deux types de substituants sont liés à un atome d'azote peuvent être appelés alkylarylamines). Les amines importantes comprennent les acides aminés, les amines biogènes, la triméthylamine et l'aniline ; voir Category:Amines pour une liste d'amines. Les dérivés inorganiques de l'ammoniac sont également appelés amines, comme la monochloramine (NClH 2 ). | |
| Acide 2-aminoisobutyrique : L'acide 2-aminoisobutyrique (également connu sous le nom d' acide α-aminoisobutyrique , AIB , -méthylalanine ou 2-méthylalanine ) est l'acide aminé non protéinogène de formule structurelle H 2 NC(CH 3 ) 2 -COOH. Il est rare dans la nature, n'ayant été trouvé que dans les météorites, et certains antibiotiques d'origine fongique, tels que l'alaméthicine et certains lantibiotiques. | 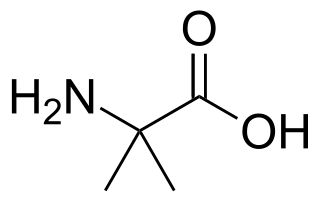 |
| Acide aminolévulinique synthase : L'acide aminolévulinique synthase ( ALA synthase , ALAS ou delta-aminolévulinique synthase ) est une enzyme (EC 2.3.1.37 ) qui catalyse la synthèse de l'acide δ-aminolévulinique (ALA) le premier précurseur commun dans la biosynthèse de tous les tétrapyrroles tels que les hèmes , cobalamines et chlorophylles. La réaction est la suivante :
| 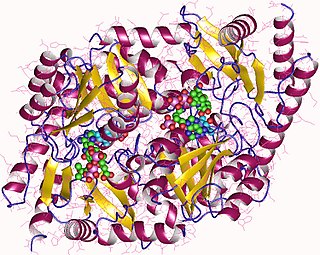 |
| Amine: En chimie organique, les amines (, UK également ) sont des composés et des groupes fonctionnels qui contiennent un atome d'azote basique avec une seule paire. Les amines sont formellement des dérivés de l'ammoniac, dans lesquels un ou plusieurs atomes d'hydrogène ont été remplacés par un substituant tel qu'un groupe alkyle ou aryle (ceux-ci peuvent être respectivement appelés alkylamines et arylamines ; les amines dans lesquelles les deux types de substituants sont liés à un atome d'azote peuvent être appelés alkylarylamines). Les amines importantes comprennent les acides aminés, les amines biogènes, la triméthylamine et l'aniline ; voir Category:Amines pour une liste d'amines. Les dérivés inorganiques de l'ammoniac sont également appelés amines, comme la monochloramine (NClH 2 ). | |
| Radical aminé : Le radical amino , • | |
| Sucre aminé : En chimie organique, un sucre aminé est une molécule de sucre dans laquelle un groupe hydroxyle a été remplacé par un groupe amine. Plus de 60 sucres aminés sont connus, l'un des plus abondants étant la N- acétyl- d- glucosamine , qui est le composant principal de la chitine. | 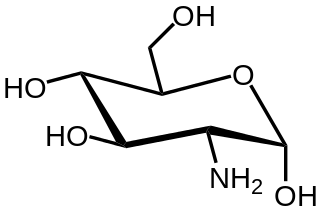 |
| Sucre aminé : En chimie organique, un sucre aminé est une molécule de sucre dans laquelle un groupe hydroxyle a été remplacé par un groupe amine. Plus de 60 sucres aminés sont connus, l'un des plus abondants étant la N- acétyl- d- glucosamine , qui est le composant principal de la chitine. |  |
| Sucre aminé : En chimie organique, un sucre aminé est une molécule de sucre dans laquelle un groupe hydroxyle a été remplacé par un groupe amine. Plus de 60 sucres aminés sont connus, l'un des plus abondants étant la N- acétyl- d- glucosamine , qui est le composant principal de la chitine. |  |
| Aspartame : L'aspartame est un édulcorant artificiel sans saccharide 200 fois plus sucré que le saccharose et est couramment utilisé comme substitut du sucre dans les aliments et les boissons. C'est un ester méthylique du dipeptide acide aspartique/phénylalanine avec les noms commerciaux NutraSweet , Equal et Canderel . L'aspartame a été fabriqué pour la première fois en 1965 et approuvé pour une utilisation dans les produits alimentaires par la Food and Drug Administration (FDA) des États-Unis en 1981. | 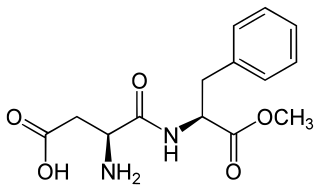 |
| N-terminal : L' extrémité N-terminale (également connue sous le nom d'extrémité aminée , extrémité NH 2 , extrémité N-terminale ou extrémité amine ) est le début d'une protéine ou d'un polypeptide faisant référence au groupe amine libre (-NH 2 ) situé à l'extrémité d'un polypeptide. Dans un peptide, le groupe amine est lié à un autre groupe carboxylique dans une protéine pour en faire une chaîne, mais comme l'acide aminé terminal d'une protéine n'est connecté qu'à l'extrémité carboxy-, le groupe amine libre restant est appelé le N- terminus. Par convention, les séquences peptidiques sont écrites de l'extrémité N à l'extrémité C, de gauche à droite (dans les systèmes d'écriture LTR). Cela corrèle la direction de la traduction à la direction du texte (car lorsqu'une protéine est traduite à partir de l'ARN messager, elle est créée de l'extrémité N à l'extrémité C - des acides aminés sont ajoutés à l'extrémité carboxyle). | |
| N-terminal : L' extrémité N-terminale (également connue sous le nom d'extrémité aminée , extrémité NH 2 , extrémité N-terminale ou extrémité amine ) est le début d'une protéine ou d'un polypeptide faisant référence au groupe amine libre (-NH 2 ) situé à l'extrémité d'un polypeptide. Dans un peptide, le groupe amine est lié à un autre groupe carboxylique dans une protéine pour en faire une chaîne, mais comme l'acide aminé terminal d'une protéine n'est connecté qu'à l'extrémité carboxy-, le groupe amine libre restant est appelé le N- terminus. Par convention, les séquences peptidiques sont écrites de l'extrémité N à l'extrémité C, de gauche à droite (dans les systèmes d'écriture LTR). Cela corrèle la direction de la traduction à la direction du texte (car lorsqu'une protéine est traduite à partir de l'ARN messager, elle est créée de l'extrémité N à l'extrémité C - des acides aminés sont ajoutés à l'extrémité carboxyle). | |
| Aminal : Un aminal ou aminoacétal est un groupe fonctionnel ou un type de composé organique qui a deux groupes amine attachés au même atome de carbone : -C(NR 2 )(NR 2 )-. (Comme il est d'usage en chimie organique, R peut représenter l'hydrogène ou un groupe alkyle). |  |
| Aminoacétaldéhyde : L'aminoacétaldéhyde est le composé organique de formule OHCCH 2 NH 2 . Dans les conditions habituelles de laboratoire, il est instable et a plutôt tendance à s'auto-condenser. L'aminoacétaldéhyde diéthylacétal est un substitut stable. |  |
| Aminoacétaldéhyde diéthylacétal : L'aminoacétaldéhyde diéthylacétal est le composé organique de formule (EtO) 2 CHCH 2 NH 2 . Liquide incolore, il est utilisé comme substitut de l'aminoacétaldéhyde. | 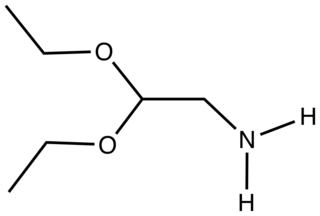 |
| Glycine : La glycine (symbole Gly ou G ; ) est un acide aminé qui a un seul atome d'hydrogène comme chaîne latérale. C'est l'acide aminé stable le plus simple (l'acide carbamique est instable), de formule chimique NH 2 ‐CH 2 ‐COOH. La glycine fait partie des acides aminés protéinogènes. Il est codé par tous les codons commençant par GG (GGU, GGC, GGA, GGG). La glycine fait partie intégrante de la formation d'hélices alpha dans la structure protéique secondaire en raison de sa forme compacte. Pour la même raison, c'est l'acide aminé le plus abondant dans les triples hélices de collagène. La glycine est également un neurotransmetteur inhibiteur - une interférence avec sa libération dans la moelle épinière (comme lors d'une infection à Clostridium tetani ) peut provoquer une paralysie spastique due à une contraction musculaire non inhibée. |  |
| Aminoacétone : L'aminoacétone est le composé organique de formule CH 3 C(O)CH 2 NH 2 . Bien que stable sous forme gazeuse, une fois condensé, il réagit avec lui-même. Le dérivé protoné forme des sels stables, par exemple le chlorhydrate d'aminoacétone ([CH 3 C(O)CH 2 NH 3 ]Cl)). La semicarbazone du chlorhydrate est un autre précurseur stable au banc. L'aminoacétone est un métabolite impliqué dans la biosynthèse du méthylglyoxal. |  |
| Aminoacétonitrile : L'aminoacétonitrile est le composé organique de formule NCCH 2 NH 2 . Le composé est un liquide incolore. Il est instable à température ambiante, en raison de l'incompatibilité du nucléophile aminé et du nitrile électrophile. Pour cette raison, il est généralement rencontré sous forme de sels chlorure et bisulfate du dérivé d'ammonium, c'est-à-dire [NCCH 2 NH 3 ] + Cl - et [NCCH 2 NH 3 ] + HSO 4 - . | |
| Acide aminé: Les acides aminés sont des composés organiques qui contiennent des groupes fonctionnels amino (-NH 2 ) et carboxyle (-COOH), ainsi qu'une chaîne latérale (groupe R) spécifique à chaque acide aminé. Les éléments clés d'un acide aminé sont le carbone (C), l'hydrogène (H), l'oxygène (O) et l'azote (N), bien que d'autres éléments se trouvent dans les chaînes latérales de certains acides aminés. Environ 500 acides aminés naturels sont connus en 1983 (bien que seulement 20 apparaissent dans le code génétique) et peuvent être classés de plusieurs manières. Ils peuvent être classés selon les emplacements des groupes fonctionnels structurels de base en acides aminés alpha- (α-) , bêta- (β-) , gamma- (γ-) ou delta- (δ-) ; d'autres catégories concernent la polarité, le niveau de pH et le type de groupe de chaînes latérales (aliphatique, acyclique, aromatique, contenant de l'hydroxyle ou du soufre, etc.). Sous forme de protéines, les résidus d'acides aminés forment le deuxième composant en importance (l'eau est le plus important) des muscles et autres tissus humains. Au-delà de leur rôle de résidus dans les protéines, les acides aminés participent à un certain nombre de processus tels que le transport et la biosynthèse des neurotransmetteurs. |  |
| Acide aminé: Les acides aminés sont des composés organiques qui contiennent des groupes fonctionnels amino (-NH 2 ) et carboxyle (-COOH), ainsi qu'une chaîne latérale (groupe R) spécifique à chaque acide aminé. Les éléments clés d'un acide aminé sont le carbone (C), l'hydrogène (H), l'oxygène (O) et l'azote (N), bien que d'autres éléments se trouvent dans les chaînes latérales de certains acides aminés. Environ 500 acides aminés naturels sont connus en 1983 (bien que seulement 20 apparaissent dans le code génétique) et peuvent être classés de plusieurs manières. Ils peuvent être classés selon les emplacements des groupes fonctionnels structurels de base en acides aminés alpha- (α-) , bêta- (β-) , gamma- (γ-) ou delta- (δ-) ; d'autres catégories concernent la polarité, le niveau de pH et le type de groupe de chaînes latérales (aliphatique, acyclique, aromatique, contenant de l'hydroxyle ou du soufre, etc.). Sous forme de protéines, les résidus d'acides aminés forment le deuxième composant en importance (l'eau est le plus important) des muscles et autres tissus humains. Au-delà de leur rôle de résidus dans les protéines, les acides aminés participent à un certain nombre de processus tels que le transport et la biosynthèse des neurotransmetteurs. |  |
| Aminoacidurie : L'aminoacidurie survient lorsque l'urine contient des quantités anormalement élevées d'acides aminés. Dans le rein sain, les glomérules filtrent tous les acides aminés du sang, et les tubules rénaux réabsorbent ensuite plus de 95 % des acides aminés filtrés dans le sang. |  |
| Aminoacidurie : L'aminoacidurie survient lorsque l'urine contient des quantités anormalement élevées d'acides aminés. Dans le rein sain, les glomérules filtrent tous les acides aminés du sang, et les tubules rénaux réabsorbent ensuite plus de 95 % des acides aminés filtrés dans le sang. |  |
| Aminoacridine : L'aminoacridine peut faire référence à l'un de plusieurs composés chimiques :
| |
| Aminoacridine : L'aminoacridine peut faire référence à l'un de plusieurs composés chimiques :
| |
| Acide aminé: Les acides aminés sont des composés organiques qui contiennent des groupes fonctionnels amino (-NH 2 ) et carboxyle (-COOH), ainsi qu'une chaîne latérale (groupe R) spécifique à chaque acide aminé. Les éléments clés d'un acide aminé sont le carbone (C), l'hydrogène (H), l'oxygène (O) et l'azote (N), bien que d'autres éléments se trouvent dans les chaînes latérales de certains acides aminés. Environ 500 acides aminés naturels sont connus en 1983 (bien que seulement 20 apparaissent dans le code génétique) et peuvent être classés de plusieurs manières. Ils peuvent être classés selon les emplacements des groupes fonctionnels structurels de base en acides aminés alpha- (α-) , bêta- (β-) , gamma- (γ-) ou delta- (δ-) ; d'autres catégories concernent la polarité, le niveau de pH et le type de groupe de chaînes latérales (aliphatique, acyclique, aromatique, contenant de l'hydroxyle ou du soufre, etc.). Sous forme de protéines, les résidus d'acides aminés forment le deuxième composant en importance (l'eau est le plus important) des muscles et autres tissus humains. Au-delà de leur rôle de résidus dans les protéines, les acides aminés participent à un certain nombre de processus tels que le transport et la biosynthèse des neurotransmetteurs. |  |
| X-Sa dipeptidase : La dipeptidase Xaa-His est une enzyme. Cette enzyme catalyse la réaction chimique suivante
| |
| Carnosinémie : La carnosinémie est une maladie métabolique autosomique récessive rare causée par un déficit en carnosinase, une dipeptidase. |  |
| X-Arg dipeptidase : La Xaa-Arg dipeptidase est une enzyme. Cette enzyme catalyse la réaction chimique suivante
| |
| X-méthyl-His dipeptidase : La Xaa-méthyl-His dipeptidase est une enzyme. Cette enzyme catalyse la réaction chimique suivante
| |
| X-méthyl-His dipeptidase : La Xaa-méthyl-His dipeptidase est une enzyme. Cette enzyme catalyse la réaction chimique suivante
| |
| Aminoacyl-ARNt : L'aminoacyl-ARNt est un ARNt auquel son acide aminé apparenté est chimiquement lié (chargé). L'aa-ARNt, ainsi que des facteurs d'élongation particuliers, livrent l'acide aminé au ribosome pour l'incorporation dans la chaîne polypeptidique qui est produite pendant la traduction. |  |
| Aminoacyl-ARNt hydrolase : En enzymologie, une aminoacyl-ARNt hydrolase (EC 3.1.1.29 ) est une enzyme qui catalyse la réaction chimique
| |
| Aminoacyl-ARNt hydrolase : En enzymologie, une aminoacyl-ARNt hydrolase (EC 3.1.1.29 ) est une enzyme qui catalyse la réaction chimique
| |
| Aminoacyl ARNt synthétase : Une aminoacyl-ARNt synthétase , également appelée ARNt-ligase, est une enzyme qui fixe l'acide aminé approprié sur son ARNt correspondant. Il le fait en catalysant la transestérification d'un acide aminé apparenté spécifique ou de son précurseur à l'un de tous ses ARNt apparentés compatibles pour former un aminoacyl-ARNt. Chez l'homme, les 20 types différents d'aa-ARNt sont fabriqués par les 20 différentes aminoacyl-ARNt synthétases, une pour chaque acide aminé du code génétique. |  |
| Aminoacyl ARNt synthétase : Une aminoacyl-ARNt synthétase , également appelée ARNt-ligase, est une enzyme qui fixe l'acide aminé approprié sur son ARNt correspondant. Il le fait en catalysant la transestérification d'un acide aminé apparenté spécifique ou de son précurseur à l'un de tous ses ARNt apparentés compatibles pour former un aminoacyl-ARNt. Chez l'homme, les 20 types différents d'aa-ARNt sont fabriqués par les 20 différentes aminoacyl-ARNt synthétases, une pour chaque acide aminé du code génétique. |  |
| Ribosomes : Les ribosomes sont des machines macromoléculaires, présentes dans toutes les cellules vivantes, qui effectuent la synthèse biologique des protéines. Les ribosomes relient les acides aminés dans l'ordre spécifié par les codons des molécules d'ARN messager (ARNm) pour former des chaînes polypeptidiques. Les ribosomes se composent de deux composants principaux : les petites et les grandes sous-unités ribosomiques. Chaque sous-unité est constituée d'une ou plusieurs molécules d'ARN ribosomique (ARNr) et de nombreuses protéines ribosomiques. Les ribosomes et les molécules associées sont également connus sous le nom d' appareil traductionnel . |  |
| Aminoacyl-ARNt : L'aminoacyl-ARNt est un ARNt auquel son acide aminé apparenté est chimiquement lié (chargé). L'aa-ARNt, ainsi que des facteurs d'élongation particuliers, livrent l'acide aminé au ribosome pour l'incorporation dans la chaîne polypeptidique qui est produite pendant la traduction. |  |
| Aminoacyl ARNt synthétase : Une aminoacyl-ARNt synthétase , également appelée ARNt-ligase, est une enzyme qui fixe l'acide aminé approprié sur son ARNt correspondant. Il le fait en catalysant la transestérification d'un acide aminé apparenté spécifique ou de son précurseur à l'un de tous ses ARNt apparentés compatibles pour former un aminoacyl-ARNt. Chez l'homme, les 20 types différents d'aa-ARNt sont fabriqués par les 20 différentes aminoacyl-ARNt synthétases, une pour chaque acide aminé du code génétique. |  |
| Aminoacyl ARNt synthétase : Une aminoacyl-ARNt synthétase , également appelée ARNt-ligase, est une enzyme qui fixe l'acide aminé approprié sur son ARNt correspondant. Il le fait en catalysant la transestérification d'un acide aminé apparenté spécifique ou de son précurseur à l'un de tous ses ARNt apparentés compatibles pour former un aminoacyl-ARNt. Chez l'homme, les 20 types différents d'aa-ARNt sont fabriqués par les 20 différentes aminoacyl-ARNt synthétases, une pour chaque acide aminé du code génétique. |  |
| Aminoacyl ARNt synthétase : Une aminoacyl-ARNt synthétase , également appelée ARNt-ligase, est une enzyme qui fixe l'acide aminé approprié sur son ARNt correspondant. Il le fait en catalysant la transestérification d'un acide aminé apparenté spécifique ou de son précurseur à l'un de tous ses ARNt apparentés compatibles pour former un aminoacyl-ARNt. Chez l'homme, les 20 types différents d'aa-ARNt sont fabriqués par les 20 différentes aminoacyl-ARNt synthétases, une pour chaque acide aminé du code génétique. |  |
| Aminoacyl ARNt synthétase : Une aminoacyl-ARNt synthétase , également appelée ARNt-ligase, est une enzyme qui fixe l'acide aminé approprié sur son ARNt correspondant. Il le fait en catalysant la transestérification d'un acide aminé apparenté spécifique ou de son précurseur à l'un de tous ses ARNt apparentés compatibles pour former un aminoacyl-ARNt. Chez l'homme, les 20 types différents d'aa-ARNt sont fabriqués par les 20 différentes aminoacyl-ARNt synthétases, une pour chaque acide aminé du code génétique. |  |
| Aminoacyl ARNt synthétase : Une aminoacyl-ARNt synthétase , également appelée ARNt-ligase, est une enzyme qui fixe l'acide aminé approprié sur son ARNt correspondant. Il le fait en catalysant la transestérification d'un acide aminé apparenté spécifique ou de son précurseur à l'un de tous ses ARNt apparentés compatibles pour former un aminoacyl-ARNt. Chez l'homme, les 20 types différents d'aa-ARNt sont fabriqués par les 20 différentes aminoacyl-ARNt synthétases, une pour chaque acide aminé du code génétique. |  |
| Aminoacyl ARNt synthétases, classe I : Les aminoacyl-ARNt synthétases catalysent la fixation d'un acide aminé à sa molécule d'ARN de transfert apparentée dans une réaction en deux étapes hautement spécifique. Ces protéines diffèrent largement par la taille et l'état oligomère, et ont une homologie de séquence limitée. Les 20 aminoacyl-ARNt synthétases sont divisées en deux classes, I et II. Les aminoacyl-ARNt synthétases de classe I contiennent un domaine catalytique de repli de Rossmann caractéristique et sont pour la plupart monomériques. Les aminoacyl-ARNt synthétases de classe II partagent un pli anti-feuillet bêta parallèle flanqué d'hélices alpha, et sont pour la plupart dimères ou multimères, contenant au moins trois régions conservées. Cependant, la liaison à l'ARNt implique une structure en hélice alpha qui est conservée entre les synthétases de classe I et de classe II. Dans les réactions catalysées par les aminoacyl-ARNt synthétases de classe I, le groupe aminoacyle est couplé au 2'-hydroxyle de l'ARNt, tandis que, dans les réactions de classe II, le site 3'-hydroxyle est préféré. Les synthétases spécifiques de l'arginine, de la cystéine, de l'acide glutamique, de la glutamine, de l'isoleucine, de la leucine, de la méthionine, de la tyrosine, du tryptophane et de la valine appartiennent aux synthétases de classe I ; ces synthétases sont en outre divisées en trois sous-classes, a, b et c, selon l'homologie de séquence. Les synthétases spécifiques de l'alanine, de l'asparagine, de l'acide aspartique, de la glycine, de l'histidine, de la lysine, de la phénylalanine, de la proline, de la sérine et de la thréonine appartiennent aux synthétases de classe II. | |
| Aminoacyl ARNt synthétases, classe II : Les aminoacyl-ARNt synthétases, classe II sont une famille de protéines. Ces protéines catalysent la fixation d'un acide aminé à sa molécule d'ARN de transfert apparentée dans une réaction en deux étapes hautement spécifique. Ces protéines diffèrent largement par la taille et l'état oligomère, et ont une homologie de séquence limitée. | |
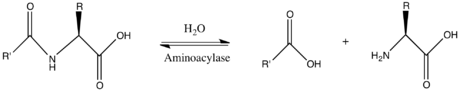
| Aminoacylase : En enzymologie, une aminoacylase (EC 3.5.1.14 ) est une enzyme qui catalyse la réaction chimique
| |
| Déficit en aminoacylase 1 : Le déficit en aminoacylase 1 est une erreur innée rare du métabolisme. À ce jour, seuls 21 cas ont été décrits. | 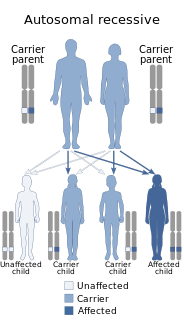 |
| Maladie de Canavan : La maladie de Canavan , ou maladie de Canavan-Van Bogaert-Bertrand, est une maladie dégénérative autosomique récessive rare et mortelle qui provoque des dommages progressifs aux cellules nerveuses et une perte de substance blanche dans le cerveau. C'est l'une des maladies cérébrales dégénératives les plus courantes de l'enfance. Elle est causée par une déficience de l'enzyme aminoacylase 2 et fait partie d'un groupe de maladies génétiques appelées leucodystrophies. Elle se caractérise par une dégénérescence de la myéline dans la couche de phospholipides isolant l'axone d'un neurone et est associée à un gène situé sur le chromosome humain 17. | |
| Aspartoacylase : L'aspartoacylase est une enzyme hydrolase qui, chez l'homme, est codée par le gène ASPA . L'ASPA est responsable de la catalyse de la désacylation du N -acétyl-l-aspartate ( N-acétylaspartate) en aspartate et acétate. C'est une hydrolase dépendante du zinc qui favorise la déprotonation de l'eau à utiliser comme nucléophile dans un mécanisme analogue à de nombreuses autres hydrolases dépendantes du zinc. Il se trouve le plus souvent dans le cerveau, où il contrôle les niveaux de N-acétyl-l-aspartate. Les mutations qui entraînent une perte d'activité de l'aspartoacylase sont associées à la maladie de Canavan, une maladie neurodégénérative autosomique récessive rare. |  |
| Aminoacylation : L'aminoacylation est le processus d'ajout d'un groupe aminoacyle à un composé. | |
| X-Sa dipeptidase : La dipeptidase Xaa-His est une enzyme. Cette enzyme catalyse la réaction chimique suivante
| |
| Synthèse peptidique : En chimie organique, la synthèse peptidique est la production de peptides, des composés où plusieurs acides aminés sont liés par des liaisons amides, également appelées liaisons peptidiques. Les peptides sont synthétisés chimiquement par la réaction de condensation du groupe carboxyle d'un acide aminé au groupe amino d'un autre. Des stratégies de groupes protecteurs sont généralement nécessaires pour empêcher des réactions secondaires indésirables avec les diverses chaînes latérales d'acides aminés. La synthèse chimique des peptides commence le plus souvent à l'extrémité carboxyle du peptide (extrémité C) et se poursuit vers l'extrémité amino (extrémité N). La biosynthèse des protéines dans les organismes vivants se produit dans la direction opposée. |  |
| Xaa-Pro aminopeptidase : Xaa-Pro aminopeptidase est une enzyme. Cette enzyme catalyse la réaction chimique suivante
| |
| Lysosomal Pro-X carboxypeptidase : La carboxypeptidase lysosomale Pro-Xaa est une enzyme. Cette enzyme catalyse la réaction chimique suivante
| |
| Aminoacyltransférase : Les aminoacyltransférases sont des enzymes acyltransférases qui agissent sur un groupe amino. Par exemple, les aminoacyl ARNt synthétases attachent un acide aminé par estérification à leur ARNt correspondant. L'activation des acides aminés avec l'aminoacyl-ARNt synthétase nécessite l'hydrolyse de l'ATP en AMP plus PP i . La molécule d'aminoacyl-ARNt a des relations étroites avec des facteurs d'élongation comme EF-Tu. |  |
| Aminoacyltransférase : Les aminoacyltransférases sont des enzymes acyltransférases qui agissent sur un groupe amino. Par exemple, les aminoacyl ARNt synthétases attachent un acide aminé par estérification à leur ARNt correspondant. L'activation des acides aminés avec l'aminoacyl-ARNt synthétase nécessite l'hydrolyse de l'ATP en AMP plus PP i . La molécule d'aminoacyl-ARNt a des relations étroites avec des facteurs d'élongation comme EF-Tu. |  |
| 2,6-Diaminopurine : La 2,6-diaminopurine est un composé autrefois utilisé dans le traitement de la leucémie. On le trouve à la place de l'adénine dans le matériel génétique de certains virus bactériophages. |  |
| Aminoadipate-semialdéhyde déshydrogénase : L'aminoadipate-semialdéhyde déshydrogénase est une protéine qui, chez l'homme, est codée par le gène AASDH. | 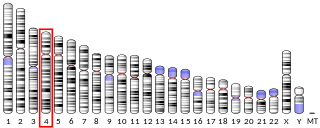 |
| 2-aminoadipate transaminase : En enzymologie, une 2-aminoadipate transaminase est une enzyme qui catalyse la réaction chimique
| |
| Alcanolamine : Les alcanolamines sont des composés chimiques qui contiennent à la fois des groupes fonctionnels hydroxyle (-OH) et amino (-NH 2 , -NHR et -NR 2 ) sur un squelette alcane. Le terme alcanolamine est un terme de classe large qui est parfois utilisé comme sous-classification. | |
| Aminoaldéhydes et aminocétones : Les aminoaldéhydes et les aminocétones sont des composés organiques qui contiennent une fonction amine ainsi qu'une fonction aldéhyde ou cétone. Ces composés sont importants en biologie et en synthèse chimique. En raison de leur nature bifonctionnelle, ils ont beaucoup attiré l'attention des chimistes. | |
| Aminoaldéhydes et aminocétones : Les aminoaldéhydes et les aminocétones sont des composés organiques qui contiennent une fonction amine ainsi qu'une fonction aldéhyde ou cétone. Ces composés sont importants en biologie et en synthèse chimique. En raison de leur nature bifonctionnelle, ils ont beaucoup attiré l'attention des chimistes. | |
| Aminoalkylindole : Les aminoalkylindoles ( AAI ) sont une famille de composés cannabinergiques qui agissent comme agoniste des récepteurs cannabinoïdes. Ils ont été inventés par la société pharmaceutique Sterling-Winthrop au début des années 1990 en tant qu'agents anti-inflammatoires non stéroïdiens potentiels. | |
| Aminoalkylindole : Les aminoalkylindoles ( AAI ) sont une famille de composés cannabinergiques qui agissent comme agoniste des récepteurs cannabinoïdes. Ils ont été inventés par la société pharmaceutique Sterling-Winthrop au début des années 1990 en tant qu'agents anti-inflammatoires non stéroïdiens potentiels. | |
| Aminoallyl nucléotide : Le nucléotide aminoallyle est un nucléotide à base modifiée contenant une allylamine. Ils sont utilisés en post-marquage d'acides nucléiques par détection de fluorescence en microarray. Ils sont réactifs avec le groupe ester N-hydroxysuccinimide qui aide à attacher un colorant fluorescent au groupe amino primaire sur le nucléotide. Ces nucléotides sont connus sous le nom de 5-(3-aminoallyl)-nucléotides puisque le groupe aminoallyle est généralement attaché au carbone 5 du cycle pyrimidine de l'uracile ou de la cytosine. Le groupe amine primaire dans la fraction aminoallyle est aliphatique et donc plus réactif par rapport aux groupes amine qui sont directement attachés aux cycles (aromatiques) des bases. Les noms communs des nucléosides d'aminoallyle sont initialement abrégés par aa- ou AA- pour indiquer l'aminoallyle. Le sucre à 5 carbones est indiqué avec ou sans le "d" minuscule indiquant le désoxyribose s'il est inclus ou le ribose sinon. Enfin la base azotée et le nombre de phosphates sont indiqués. |  |
| Aminoallyl nucléotide : Le nucléotide aminoallyle est un nucléotide à base modifiée contenant une allylamine. Ils sont utilisés en post-marquage d'acides nucléiques par détection de fluorescence en microarray. Ils sont réactifs avec le groupe ester N-hydroxysuccinimide qui aide à attacher un colorant fluorescent au groupe amino primaire sur le nucléotide. Ces nucléotides sont connus sous le nom de 5-(3-aminoallyl)-nucléotides puisque le groupe aminoallyle est généralement attaché au carbone 5 du cycle pyrimidine de l'uracile ou de la cytosine. Le groupe amine primaire dans la fraction aminoallyle est aliphatique et donc plus réactif par rapport aux groupes amine qui sont directement attachés aux cycles (aromatiques) des bases. Les noms communs des nucléosides d'aminoallyle sont initialement abrégés par aa- ou AA- pour indiquer l'aminoallyle. Le sucre à 5 carbones est indiqué avec ou sans le "d" minuscule indiquant le désoxyribose s'il est inclus ou le ribose sinon. Enfin la base azotée et le nombre de phosphates sont indiqués. |  |
| Ampyrone : L'ampyrone est un métabolite de l'aminopyrine aux propriétés analgésiques, anti-inflammatoires et antipyrétiques. En raison du risque d'agranulocytose, son utilisation en tant que médicament est déconseillée. Il est utilisé comme réactif pour des réactions biochimiques produisant des peroxydes ou des phénols. L'ampyrone stimule les microsomes hépatiques et est également utilisée pour mesurer l'eau extracellulaire. |  |
| Colorant azoïque : Les colorants azoïques sont des composés organiques portant le groupement fonctionnel R-N=N-R′, dans lequel R et R′ sont généralement un aryle. Il s'agit d'une famille commercialement importante de composés azoïques, c'est-à-dire de composés contenant la liaison CN=NC. Les colorants azoïques sont largement utilisés pour traiter les textiles, les articles en cuir et certains aliments. Chimiquement liés aux colorants azoïques sont les pigments azoïques, qui sont insolubles dans l'eau et d'autres solvants. |  |
| Colorant azoïque : Les colorants azoïques sont des composés organiques portant le groupement fonctionnel R-N=N-R′, dans lequel R et R′ sont généralement un aryle. Il s'agit d'une famille commercialement importante de composés azoïques, c'est-à-dire de composés contenant la liaison CN=NC. Les colorants azoïques sont largement utilisés pour traiter les textiles, les articles en cuir et certains aliments. Chimiquement liés aux colorants azoïques sont les pigments azoïques, qui sont insolubles dans l'eau et d'autres solvants. |  |
| Colorant azoïque : Les colorants azoïques sont des composés organiques portant le groupement fonctionnel R-N=N-R′, dans lequel R et R′ sont généralement un aryle. Il s'agit d'une famille commercialement importante de composés azoïques, c'est-à-dire de composés contenant la liaison CN=NC. Les colorants azoïques sont largement utilisés pour traiter les textiles, les articles en cuir et certains aliments. Chimiquement liés aux colorants azoïques sont les pigments azoïques, qui sont insolubles dans l'eau et d'autres solvants. |  |
| Jaune d'aniline : Le jaune d'aniline est un colorant azoïque jaune et une amine aromatique. C'est un dérivé de l'azobenzène. Il a l'apparence d'une poudre d'orange. Le jaune d'aniline a été le premier colorant azoïque. il a été produit pour la première fois en 1861 par C. Mene. Le deuxième colorant azoïque était le Bismarck Brown en 1863. Le jaune d'aniline a été commercialisé en 1864 en tant que premier colorant azoïque commercial, un an après le noir d'aniline. Il est fabriqué à partir d'aniline. |  |
| Aminobacter : Aminobacter est un genre de bactéries du sol à Gram négatif. | |
| Aminobacter aganoensis : Aminobacter aganoensis est une bactérie du genre Aminobacter qui a été isolée du sol. | |
| Aminobacter aminovorans : Aminobacter aminovorans est une bactérie du sol à Gram négatif. | |
| Aminobacter anthyllidis : Aminobacter anthyllidis est une bactérie du genre Aminobacter. | |
| Aminobacter carboxidus : Aminobacter carboxidus est une bactérie du genre Aminobacter qui a été isolée du sol à Moscou en Russie. | |
| Aminobacter ciceronei : Aminobacter ciceronei est une bactérie du genre Aminobacter qui a été isolée du sol agricole en Californie aux États-Unis. Aminobacter anthyllidis a la capacité de dégrader le chlorométhane et le bromométhane. | |
| Aminobacter lissarensis : Aminobacter lissarensis est une bactérie du genre Aminobacter qui a été isolée du sol d'une hêtraie en Irlande du Nord. | |
| Aminobacter niigataensis : Aminobacter niigataensis est une bactérie du genre Aminobacter qui a été isolée du sol. | |
| Aminobactérie : Aminobacterium est un genre de bactéries à Gram négatif de la famille des Synergistaceae. | |
| Aminobacterium colombiense : Aminobacterium colombiense est une bactérie à Gram négatif, mésophile, strictement anaérobie et non sporulée du genre Aminobacterium qui a été isolée d'une lagune anaérobie d'une usine de traitement des eaux usées laitières en Colombie. | |
| Aminobactérie mobile : Aminobacterium mobile est une bactérie à Gram négatif, anaérobie, mésophile, non sporulée et mobile du genre Aminobacterium qui a été isolée d'une lagune anaérobie d'une usine de traitement des eaux usées laitières en Colombie. Contrairement à Aminobacterium colombiense , Aminobacterium mobile a une teneur en ADN légèrement inférieure en GC. Aminobacterium mobile est mobile et fermente la sérine en acétate et en alanine. Aminobacterium mobile est à la fois hétérotrophe et asaccharolytique. Ses effets indésirables sur les animaux et les humains ne sont pas encore connus, mais en raison de la capacité d' Aminobacterium mobile à dégrader les acides aminés et les peptides, la possibilité d'effets nocifs ne peut être exclue. | |
| Aminobactérie mobile : Aminobacterium mobile est une bactérie à Gram négatif, anaérobie, mésophile, non sporulée et mobile du genre Aminobacterium qui a été isolée d'une lagune anaérobie d'une usine de traitement des eaux usées laitières en Colombie. Contrairement à Aminobacterium colombiense , Aminobacterium mobile a une teneur en ADN légèrement inférieure en GC. Aminobacterium mobile est mobile et fermente la sérine en acétate et en alanine. Aminobacterium mobile est à la fois hétérotrophe et asaccharolytique. Ses effets indésirables sur les animaux et les humains ne sont pas encore connus, mais en raison de la capacité d' Aminobacterium mobile à dégrader les acides aminés et les peptides, la possibilité d'effets nocifs ne peut être exclue. | |
| Aminobacterium thunnarium : Aminobacterium thunnarium est une bactérie à Gram négatif, anaérobie, mésophile et non sporulée du genre Aminobacterium qui a été isolée des boues. | |
| Orthocaïne : L'orthocaïne est un anesthésique local. Développé dans les années 1890, il s'est avéré d'une utilité limitée en raison de sa faible solubilité dans l'eau, mais il a été utilisé sous forme de poudre pour épousseter les plaies douloureuses. | 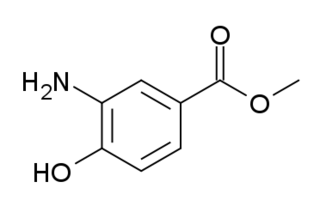 |
| Aminobenzal : En chimie organique, l' aminobenzal est un groupe fonctionnel composé d'un cétal cyclique d'un diol avec le 4-diméthylaminobenzylidène. Il est observé dans le triamcinolone aminobenzal benzamidoisobutyrate. | |
| Aminobenzal : En chimie organique, l' aminobenzal est un groupe fonctionnel composé d'un cétal cyclique d'un diol avec le 4-diméthylaminobenzylidène. Il est observé dans le triamcinolone aminobenzal benzamidoisobutyrate. | |
| Aniline: L'aniline est un composé organique de formule C 6 H 5 NH 2 . Constituée d'un groupe phényle attaché à un groupe amino, l'aniline est l'amine aromatique la plus simple. C'est un produit chimique de base d'importance industrielle, ainsi qu'un matériau de départ polyvalent pour la synthèse chimique fine. Son utilisation principale est la fabrication de précurseurs de polyuréthane, de colorants et d'autres produits chimiques industriels. Comme la plupart des amines volatiles, elle a une odeur de poisson pourri. Il s'enflamme facilement, brûlant d'une flamme fumée caractéristique des composés aromatiques. |  |
| Acide aminobenzoïque : L'acide aminobenzoïque peut désigner :
| |
| Aminobenzoate décarboxylase : En enzymologie, une aminobenzoate décarboxylase (EC 4.1.1.24 ) est une enzyme qui catalyse la réaction chimique
| |
| Aminobenzoate décarboxylase : En enzymologie, une aminobenzoate décarboxylase (EC 4.1.1.24 ) est une enzyme qui catalyse la réaction chimique
| |
| Acide aminobenzoïque : L'acide aminobenzoïque peut désigner :
| |
| Acide aminobenzoïque : L'acide aminobenzoïque peut désigner :
| |
| Acide aminobenzoïque : L'acide aminobenzoïque peut désigner :
| |
| 3-(Trifluorométhyl)aniline : La 3-(trifluorométhyl)aniline est un composé de formule moléculaire CF 3 C 6 H 4 NH 2 . C'est une amine aromatique. |  |
| Aminobiphényle : Aminobiphényle peut faire référence à :
| |
| Aminoglutéthimide : L'aminoglutéthimide ( AG ), vendu sous les noms de marque Elipten , Cytadren et Orimeten, entre autres, est un médicament qui a été utilisé dans le traitement des convulsions, du syndrome de Cushing, du cancer du sein et du cancer de la prostate, entre autres indications. Il a également été utilisé par des culturistes, des athlètes et d'autres hommes à des fins de renforcement musculaire et d'amélioration de la performance et du physique. AG est pris par voie orale trois ou quatre fois par jour. |  |
| Butylamine : La butylamine peut faire référence à l'un de plusieurs composés chimiques apparentés :
| |
| Aminobutyraldéhyde déshydrogénase : En enzymologie, une aminobutyraldéhyde déshydrogénase (EC 1.2.1.19 ) est une enzyme qui catalyse la réaction chimique
| |
| Acide aminobutyrique : L'acide aminobutyrique peut faire référence à l'un des trois composés chimiques isomères :
| |
| Aminobutyrate aminotransférase : Aminobutyrate aminotransférase peut désigner :
| |
| 4-aminobutyrate—pyruvate transaminase : 4-aminobutyrate --- pyruvate transaminase est une enzyme avec le nom systématique 4-aminobutanoate:pyruvate aminotransférase . Cette enzyme est un type de GABA transaminase, qui dégrade le neurotransmetteur GABA. L'enzyme catalyse la réaction chimique suivante
| |
| Acide aminobutyrique : L'acide aminobutyrique peut faire référence à l'un des trois composés chimiques isomères :
| |
| Acide aminobutyrique : L'acide aminobutyrique peut faire référence à l'un des trois composés chimiques isomères :
| |
| Aminocandine : L'aminocandine est un antifongique échinocandine. Il agit en ciblant le glucane dans les parois cellulaires fongiques. |  |
| Acide aminocaproïque : L'acide aminocaproïque est un dérivé et un analogue de l'acide aminé lysine, ce qui en fait un inhibiteur efficace des enzymes qui se lient à ce résidu particulier. De telles enzymes comprennent des enzymes protéolytiques comme la plasmine, l'enzyme responsable de la fibrinolyse. Pour cette raison, il est efficace dans le traitement de certains troubles de la coagulation et il est vendu sous le nom de marque Amicar . L'acide aminocaproïque est également un intermédiaire dans la polymérisation du Nylon-6, où il est formé par hydrolyse par ouverture de cycle du caprolactame. La détermination de la structure cristalline a montré que l'acide 6-aminohexanoïque est présent sous forme de sel, au moins à l'état solide. |  |
| Acide aminocaproïque : L'acide aminocaproïque est un dérivé et un analogue de l'acide aminé lysine, ce qui en fait un inhibiteur efficace des enzymes qui se lient à ce résidu particulier. De telles enzymes comprennent des enzymes protéolytiques comme la plasmine, l'enzyme responsable de la fibrinolyse. Pour cette raison, il est efficace dans le traitement de certains troubles de la coagulation et il est vendu sous le nom de marque Amicar . L'acide aminocaproïque est également un intermédiaire dans la polymérisation du Nylon-6, où il est formé par hydrolyse par ouverture de cycle du caprolactame. La détermination de la structure cristalline a montré que l'acide 6-aminohexanoïque est présent sous forme de sel, au moins à l'état solide. |  |
Rechercher dans ce blog
jeudi 3 juin 2021
Amino acid, Branched-chain amino acid, Essential amino acid
Inscription à :
Publier les commentaires (Atom)
-
Akim Swedru (circonscription parlementaire du Ghana): Akim Swedru est l'une des circonscriptions représentées au Parlement du Ghan...
-
Antanartia délius : Antanartia delius , l' amiral des forêts ou amiral orange , est un papillon de la famille des Nymphalidae. ...
-
Rallye d'Akademos: L' Akademos Rally est un rallye automobile annuel organisé à Victoria, en Australie, par le Melbourne Unive...

Aucun commentaire:
Enregistrer un commentaire