| 2-Heptanone : La 2-heptanone , également connue sous le nom de méthyl n -amyl cétone , ou Heptan-2-one , est une cétone de formule moléculaire C 7 H 14 O. C'est un liquide incolore ressemblant à de l'eau avec une odeur fruitée de banane. . La 2-heptanone a une charge formelle neutre et n'est que légèrement soluble dans l'eau. |  |
| Nitrate d'amyle : Le nitrate d'amyle est le composé chimique de formule CH 3 (CH 2 ) 4 ONO 2 . Cette molécule est constituée du groupe amyle à 5 atomes de carbone attaché à une fonction nitrate. C'est l'ester d'alcool amylique et d'acide nitrique. |  |
| Nitrate d'amyle : Le nitrate d'amyle est le composé chimique de formule CH 3 (CH 2 ) 4 ONO 2 . Cette molécule est constituée du groupe amyle à 5 atomes de carbone attaché à une fonction nitrate. C'est l'ester d'alcool amylique et d'acide nitrique. |  |
| Nitrite d'amyle : Le nitrite d'amyle est un composé chimique de formule C 5 H 11 ONO. Une variété d'isomères sont connus, mais ils comportent tous un groupe amyle attaché au groupe fonctionnel nitrite. Le groupe alkyle n'est pas réactif et les propriétés chimiques et biologiques sont principalement dues au groupe nitrite. Comme les autres nitrites d'alkyle, le nitrite d'amyle est bioactif chez les mammifères, étant un vasodilatateur, ce qui est à la base de son utilisation en tant que médicament d'ordonnance. En tant qu'inhalant, il a également un effet psychoactif, ce qui a conduit à son utilisation récréative avec son odeur décrite comme celle de vieilles chaussettes ou de pieds sales. Il est également appelé gaz banapple . |  |
| Pentyle pentanoate : Le pentanoate de pentyle (C 4 H 9 COOC 5 H 11 ) est un ester utilisé en solution diluée pour reproduire l'odeur ou la saveur de la pomme, et parfois de l'ananas. Il est appelé valérate de pentyle ou pentanoate d'amyle selon la nomenclature classique. il peut être utilisé pour une variété d'utilisations chimiques, comme dans la production de produits aromatisés, comme les bonbons. | |
| Propanoate de pentyle : Le propanoate de pentyle est un ester organique formé par la condensation de pentan-1-ol et d'acide propanoïque. C'est un liquide incolore avec une odeur de pomme, qui flotte sur l'eau. | |
| Pentyle pentanoate : Le pentanoate de pentyle (C 4 H 9 COOC 5 H 11 ) est un ester utilisé en solution diluée pour reproduire l'odeur ou la saveur de la pomme, et parfois de l'ananas. Il est appelé valérate de pentyle ou pentanoate d'amyle selon la nomenclature classique. il peut être utilisé pour une variété d'utilisations chimiques, comme dans la production de produits aromatisés, comme les bonbons. | |
| Pentyle pentanoate : Le pentanoate de pentyle (C 4 H 9 COOC 5 H 11 ) est un ester utilisé en solution diluée pour reproduire l'odeur ou la saveur de la pomme, et parfois de l'ananas. Il est appelé valérate de pentyle ou pentanoate d'amyle selon la nomenclature classique. il peut être utilisé pour une variété d'utilisations chimiques, comme dans la production de produits aromatisés, comme les bonbons. | |
| Pentyle pentanoate : Le pentanoate de pentyle (C 4 H 9 COOC 5 H 11 ) est un ester utilisé en solution diluée pour reproduire l'odeur ou la saveur de la pomme, et parfois de l'ananas. Il est appelé valérate de pentyle ou pentanoate d'amyle selon la nomenclature classique. il peut être utilisé pour une variété d'utilisations chimiques, comme dans la production de produits aromatisés, comme les bonbons. | |
| 1-Octen-3-ol : 1-octène-3-ol, octénol pour court et également connu sous le nom d' alcool de champignon, est un produit chimique qui attire les insectes piqueurs tels que les moustiques. Il est contenu dans l'haleine et la sueur humaines, et on croyait autrefois que le DEET insectifuge fonctionnait en bloquant les récepteurs odorants de l'octenol des insectes. Des preuves récentes chez les moustiques Anopheles gambiae et Culex quequinfasciatius suggèrent que le DEET réduit la volatilité du 1-octène-3-ol, ce qui peut entraîner une réduction de l'attraction humaine. Le 1-octène-3-ol est un alcool secondaire dérivé du 1-octène. Il existe sous forme de deux énantiomères, le ( R )-(–)-1-octène-3-ol et ( S )-(+)-1-octène-3-ol. |  |
| Acétate de 1-octén-3-yle : L'acétate de 1-octén-3-yle est un composé chimique de formule moléculaire C 10 H 18 O 2 . C'est un ester d'acide acétique et d'oct-1-en-3-ol. Il existe sous forme de deux énantiomères et peut être obtenu sous forme de mélange racémique. C'est un composant de l'huile de lavande. |  |
| LPMud : LPMud , en abrégé LP , est une famille de logiciels de serveur MUD. Sa première instance, le pilote de jeu original LPMud, a été développé en 1989 par Lars Pensjö. LPMud était innovant dans sa séparation de l'infrastructure MUD en une machine virtuelle et un cadre de développement écrit dans le langage de programmation LPC. | |
| Amylacée : Amylacée peut désigner :
| |
| Amylacée : Amylacée peut désigner :
| |
| Acétate d'amyle : L'acétate d'amyle ( acétate de pentyle ) est un composé organique et un ester de formule chimique CH 3 COO[CH 2 ] 4 CH 3 et de poids moléculaire 130,19 g/mol. Il a une odeur semblable aux bananes et aux pommes. Le composé est le produit de condensation de l'acide acétique et du 1-pentanol. Cependant, les esters formés à partir d'autres isomères du pentanol (alcools amyliques) ou de mélanges de pentanols sont souvent appelés acétate d'amyle. | 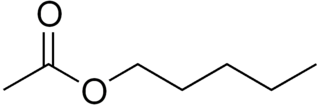 |
| Castor et Pollux : Castor et Pollux sont des demi-frères jumeaux dans la mythologie grecque et romaine, connus ensemble sous le nom de Dioscures . |  |
| 1-Aminopentane : Le 1-aminopentane est un composé organique de formule CH 3 (CH 2 ) 4 NH 2 . Il est utilisé comme solvant, comme matière première dans la fabrication d'une variété d'autres composés, notamment des colorants, des émulsifiants et des produits pharmaceutiques, et comme agent aromatisant. | |
| Amylaire : Amylaria est un genre de champignon de la famille des Bondarzewiaceae. Le genre est monotypique, contenant la seule espèce Amylaria himalayensis , trouvée au Bhoutan. | |
| Amylaire : Amylaria est un genre de champignon de la famille des Bondarzewiaceae. Le genre est monotypique, contenant la seule espèce Amylaria himalayensis , trouvée au Bhoutan. | |
| Amylasque : Amylascus est un genre de champignons ressemblant à des truffes de la famille des Pezizaceae. Le genre, qui contient deux espèces trouvées en Australasie, a été circonscrit par le mycologue James Trappe en 1971. | |
| Amylase : Une amylase est une enzyme qui catalyse l'hydrolyse de l'amidon en sucres. L'amylase est présente dans la salive des humains et de certains autres mammifères, où elle commence le processus chimique de digestion. Les aliments qui contiennent de grandes quantités d'amidon mais peu de sucre, comme le riz et les pommes de terre, peuvent acquérir un goût légèrement sucré lorsqu'ils sont mâchés car l'amylase dégrade une partie de leur amidon en sucre. Le pancréas et la glande salivaire fabriquent de l'amylase pour hydrolyser l'amidon alimentaire en disaccharides et trisaccharides qui sont convertis par d'autres enzymes en glucose pour fournir de l'énergie au corps. Les plantes et certaines bactéries produisent également de l'amylase. Les protéines amylases spécifiques sont désignées par différentes lettres grecques. Toutes les amylases sont des glycoside hydrolases et agissent sur les liaisons α-1,4-glycosidiques. | 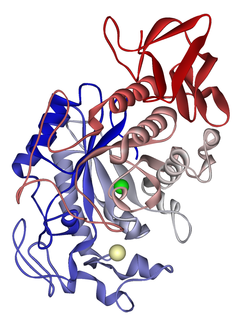 |
| Amylase : Une amylase est une enzyme qui catalyse l'hydrolyse de l'amidon en sucres. L'amylase est présente dans la salive des humains et de certains autres mammifères, où elle commence le processus chimique de digestion. Les aliments qui contiennent de grandes quantités d'amidon mais peu de sucre, comme le riz et les pommes de terre, peuvent acquérir un goût légèrement sucré lorsqu'ils sont mâchés car l'amylase dégrade une partie de leur amidon en sucre. Le pancréas et la glande salivaire fabriquent de l'amylase pour hydrolyser l'amidon alimentaire en disaccharides et trisaccharides qui sont convertis par d'autres enzymes en glucose pour fournir de l'énergie au corps. Les plantes et certaines bactéries produisent également de l'amylase. Les protéines amylases spécifiques sont désignées par différentes lettres grecques. Toutes les amylases sont des glycoside hydrolases et agissent sur les liaisons α-1,4-glycosidiques. |  |
| Amylax : Amylax est un genre de dinoflagellés appartenant à la famille des Lingulodiniaceae. | |
| Amobarbital : L'amobarbital est un médicament dérivé des barbituriques. Il a des propriétés sédatives-hypnotiques. C'est une poudre cristalline blanche sans odeur et au goût légèrement amer. Il a été synthétisé pour la première fois en Allemagne en 1923. Il est considéré comme un barbiturique à action intermédiaire. Si l'amobarbital est pris pendant des périodes prolongées, une dépendance physique et psychologique peut se développer. Le sevrage de l'amobarbital imite le delirium tremens et peut mettre la vie en danger. L'amobarbital était autrefois fabriqué par Eli Lilly and Company aux États-Unis sous le nom de marque Amytal dans des capsules en forme de balle bleu vif ou des comprimés roses contenant 50, 100 ou 200 milligrammes de médicament. Il a été largement abusé, connu sous le nom de "Heavenly Blues" dans les rues, et a été interrompu par Eli Lilly au début des années 1980. | 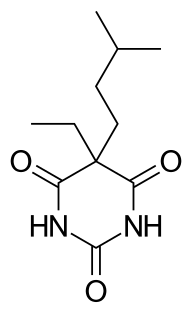 |
| Amy Lee (saxophoniste) : Amy Lee est une saxophoniste, compositrice et arrangeuse américaine. Elle a joué avec divers musiciens et chanteurs et est surtout connue pour être membre du Coral Reefer Band de Jimmy Buffett. | |
| Pentène : Les pentènes sont des alcènes de formule chimique C | 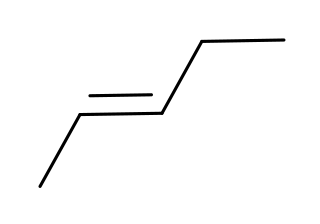 |
| Alcool tert-amylique : L'alcool tert- amylique ( TAA ) ou 2-méthylbutan-2-ol ( 2M2B ), est un pentanol ramifié. |  |
| Amylibactérie : Amylibacter est un genre de bactéries de la famille des Rhodobacteraceae. | |
| Amylibacter cionae : Amylibacter cionae est une bactérie Gram-négative, aérobie, en forme de bâtonnet et immobile du genre Amylibacter qui a été isolée de l'ascidie Ciona savignyi de la baie de Jiaozhou en Chine. | |
| Amylibacter kogurei : Amylibacter kogurei est une bactérie à Gram négatif du genre Amylibacter . | |
| Amylibacter lutimaris : Amylibacter lutimaris est une bactérie Gram-négative, aérobie et non mobile du genre Amylibacter qui a été isolée des sédiments des vasières de Corée. | |
| Amylibacter marinus : Amylibacter marinus est une bactérie Gram-négative, aérobie, mésophile et immobile du genre Amylibacter qui a été isolée de l'eau de mer près de Muroto au Japon. | |
| Amylibacter ulvae : Amylibacter ulvae est une bactérie à Gram négatif, strictement aérobie, en forme de bâtonnet et immobile du genre Amylibacter qui a été isolée de l'algue Ulva fenestrata . | |
| Amélie : Amylie Boisclair est une auteure-compositrice-interprète canadienne du Québec. Elle est surtout connue pour son album Le Royaume de 2012, qui a été nominé aux prix Juno pour l'album francophone de l'année aux prix Juno de 2013. |  |
| Amyline : L'amyline, ou polypeptide amyloïde des îlots ( IAPP ), est une hormone peptidique à 37 résidus. Il est cosécrété avec l'insuline des cellules β pancréatiques dans un rapport d'environ 100:1 (insuline:amyline). L'amyline joue un rôle dans la régulation glycémique en ralentissant la vidange gastrique et en favorisant la satiété, empêchant ainsi les pics post-prandiaux de la glycémie. |  |
| Amylin Pharmaceuticals : Amylin Pharmaceuticals était une société biopharmaceutique basée à San Diego, en Californie, qui a été fondée en 1987. La société était engagée dans la découverte, le développement et la commercialisation de candidats-médicaments pour le traitement du diabète, de l'obésité et d'autres maladies. Amylin a produit trois médicaments : Symlin, Byetta (exénatide) et Bydureon. |  |
| Amylin Pharmaceuticals : Amylin Pharmaceuticals était une société biopharmaceutique basée à San Diego, en Californie, qui a été fondée en 1987. La société était engagée dans la découverte, le développement et la commercialisation de candidats-médicaments pour le traitement du diabète, de l'obésité et d'autres maladies. Amylin a produit trois médicaments : Symlin, Byetta (exénatide) et Bydureon. |  |
| Amylin Pharmaceuticals : Amylin Pharmaceuticals était une société biopharmaceutique basée à San Diego, en Californie, qui a été fondée en 1987. La société était engagée dans la découverte, le développement et la commercialisation de candidats-médicaments pour le traitement du diabète, de l'obésité et d'autres maladies. Amylin a produit trois médicaments : Symlin, Byetta (exénatide) et Bydureon. |  |
| Famille Amyline : En biologie moléculaire, la famille des protéines amylines ou la famille des protéines calcitonine/CGRP/IAPP est une famille de protéines, qui comprend les précurseurs du peptide lié au gène de la calcitonine/calcitonine (CGRP), du polypeptide amyloïde des îlots (IAPP) et de l'adrénomédulline. |  |
| Amylose : Amylirosa est un genre de champignons de la classe des Dothideomycètes. La relation de ce taxon avec d'autres taxons au sein de la classe est inconnue. | |
| Amylis : Amylis est un genre de champignons de la classe des Sordariomycètes. La relation de ce taxon avec d'autres taxons au sein de la classe est inconnue. Il s'agit d'un genre monotypique, contenant la seule espèce Amylis memorabilis . | |
| Amylis : Amylis est un genre de champignons de la classe des Sordariomycètes. La relation de ce taxon avec d'autres taxons au sein de la classe est inconnue. Il s'agit d'un genre monotypique, contenant la seule espèce Amylis memorabilis . | |
| Amylmétacrésol : L'amylmétacrésol ( AMC ) est un antiseptique utilisé pour traiter les infections de la bouche et de la gorge. Il est utilisé comme ingrédient pharmaceutique actif dans les pastilles pour la gorge Strepsils, Cēpacol, Gorpils et Lorsept, généralement en combinaison avec de l'alcool dichlorobenzylique, un autre antiseptique. |  |
| Amylmétacrésol : L'amylmétacrésol ( AMC ) est un antiseptique utilisé pour traiter les infections de la bouche et de la gorge. Il est utilisé comme ingrédient pharmaceutique actif dans les pastilles pour la gorge Strepsils, Cēpacol, Gorpils et Lorsept, généralement en combinaison avec de l'alcool dichlorobenzylique, un autre antiseptique. |  |
| Amylo-alpha-1,6-glucosidase : L'amylo-alpha-1,6-glucosidase est une enzyme dont le nom systématique est la glycogène phosphorylase-limite dextrine 6-alpha-glucohydrolase . Cette enzyme catalyse la réaction chimique suivante
| |
| Maladie de stockage du glycogène de type III : La maladie de stockage du glycogène de type III est un trouble métabolique autosomique récessif et une erreur innée du métabolisme caractérisée par un déficit en enzymes de déramification du glycogène. | 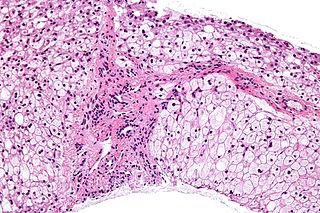 |
| Amylo-alpha-1,6-glucosidase : L'amylo-alpha-1,6-glucosidase est une enzyme dont le nom systématique est la glycogène phosphorylase-limite dextrine 6-alpha-glucohydrolase . Cette enzyme catalyse la réaction chimique suivante
| |
| Amyloathélie : L'amyloathelia est un genre de champignons de la famille des Amylocorticaceae. Le genre comprend trois espèces réparties en Europe et en Amérique du Sud. | |
| Amylobacille : Amylobacillus est un genre de bactéries de la famille des Bacillacées avec une espèce connue. | |
| Amobarbital : L'amobarbital est un médicament dérivé des barbituriques. Il a des propriétés sédatives-hypnotiques. C'est une poudre cristalline blanche sans odeur et au goût légèrement amer. Il a été synthétisé pour la première fois en Allemagne en 1923. Il est considéré comme un barbiturique à action intermédiaire. Si l'amobarbital est pris pendant des périodes prolongées, une dépendance physique et psychologique peut se développer. Le sevrage de l'amobarbital imite le delirium tremens et peut mettre la vie en danger. L'amobarbital était autrefois fabriqué par Eli Lilly and Company aux États-Unis sous le nom de marque Amytal dans des capsules en forme de balle bleu vif ou des comprimés roses contenant 50, 100 ou 200 milligrammes de médicament. Il a été largement abusé, connu sous le nom de "Heavenly Blues" dans les rues, et a été interrompu par Eli Lilly au début des années 1980. |  |
| Amobarbital : L'amobarbital est un médicament dérivé des barbituriques. Il a des propriétés sédatives-hypnotiques. C'est une poudre cristalline blanche sans odeur et au goût légèrement amer. Il a été synthétisé pour la première fois en Allemagne en 1923. Il est considéré comme un barbiturique à action intermédiaire. Si l'amobarbital est pris pendant des périodes prolongées, une dépendance physique et psychologique peut se développer. Le sevrage de l'amobarbital imite le delirium tremens et peut mettre la vie en danger. L'amobarbital était autrefois fabriqué par Eli Lilly and Company aux États-Unis sous le nom de marque Amytal dans des capsules en forme de balle bleu vif ou des comprimés roses contenant 50, 100 ou 200 milligrammes de médicament. Il a été largement abusé, connu sous le nom de "Heavenly Blues" dans les rues, et a été interrompu par Eli Lilly au début des années 1980. |  |
| Amylobasidium : Amylobasidium est un genre fongique de la famille des Corticiacées. C'est un genre monotypique, contenant la seule espèce Amylobasidium tsugae . Signalé pour la première fois par J. Ginns en 1988, il a été trouvé poussant sur le bois et dans les crevasses de l'écorce des rondins de Tsuga mertensiana des pics volcaniques de la cordillère de l'ouest de l'Amérique du Nord. | |
| Amylobasidium : Amylobasidium est un genre fongique de la famille des Corticiacées. C'est un genre monotypique, contenant la seule espèce Amylobasidium tsugae . Signalé pour la première fois par J. Ginns en 1988, il a été trouvé poussant sur le bois et dans les crevasses de l'écorce des rondins de Tsuga mertensiana des pics volcaniques de la cordillère de l'ouest de l'Amérique du Nord. | |
| Améloblaste : Les améloblastes sont des cellules présentes uniquement pendant le développement des dents qui déposent l'émail dentaire, qui est la couche externe dure de la dent formant la surface de la couronne. |  |
| Amylocaïne : L'amylocaïne a été le premier anesthésique local synthétique. Il a été synthétisé et breveté sous le nom de Stovaine par Ernest Fourneau à l'Institut Pasteur en 1903. Il était principalement utilisé en rachianesthésie. |  |
| Amylocarpe : Amylocarpus est un genre de champignons de l'ordre des Helotiales. La relation de ce taxon avec d'autres taxons au sein de l'ordre est inconnue, et il n'a encore été placé avec certitude dans aucune famille. | |
| Amylocorticales : Les amylocorticales sont un ordre de champignons de la classe des Agaricomycètes. L'ordre a été circonscrite en 2010 pour contenir la plupart des formes résupinées (croûte etc.) qui ont été visés à des genres Anomoporia, Amyloathelia, Amylocorticiellum, Amylocorticium, Amyloxenasma, Anomoloma, Athelia, Athelopsis, Ceraceomyces, Hypochniciellum, Leptosporomyces et Serpulomyces. |  |
| Amylocorticales : Les amylocorticales sont un ordre de champignons de la classe des Agaricomycètes. L'ordre a été circonscrite en 2010 pour contenir la plupart des formes résupinées (croûte etc.) qui ont été visés à des genres Anomoporia, Amyloathelia, Amylocorticiellum, Amylocorticium, Amyloxenasma, Anomoloma, Athelia, Athelopsis, Ceraceomyces, Hypochniciellum, Leptosporomyces et Serpulomyces. |  |
| Amylocorticiel : Amylocorticiellum est un genre de champignons de la famille des Amylocorticiaceae. Le genre a une distribution étendue et contient quatre espèces. | |
| Amylocorticium : Amylocorticium est un genre de champignons resupinés (ressemblant à une croûte) de la famille des Amylocorticiaceae. Le genre a une distribution étendue et contient 11 espèces. |  |
| Amylocyste : Amylocystis est un genre de deux espèces de champignons de la famille des Fomitopsidaceae. Le genre a été décrit en 1944 par les mycologues Appollinaris Semenovich Bondartsev et Rolf Singer pour contenir le type, et à l'époque, la seule espèce, A. lapponicus . A. unicolor a été transféré au genre en 2003. Le nom générique Amylocystis est dérivé des mots grecs anciens άμυλον ("amidon") et ("vessie"). |  |
| Amylocystis lapponica : Amylocystis lapponica est une espèce de champignon de support de la famille des Fomitopsidaceae, et l'espèce type du genre Amylocystis . Il produit des corps de fruits annuels de taille moyenne qui sont mous et ont une odeur forte et distincte. Le champignon est un saprophyte qui se nourrit de bois de conifères de bûches gisant sur le sol, et provoque la pourriture brune. C'est une espèce assez rare qui n'est présente que dans les forêts anciennes. |  |
| Amylocystis lapponica : Amylocystis lapponica est une espèce de champignon de support de la famille des Fomitopsidaceae, et l'espèce type du genre Amylocystis . Il produit des corps de fruits annuels de taille moyenne qui sont mous et ont une odeur forte et distincte. Le champignon est un saprophyte qui se nourrit de bois de conifères de bûches gisant sur le sol, et provoque la pourriture brune. C'est une espèce assez rare qui n'est présente que dans les forêts anciennes. |  |
| Dextrine: Les dextrines sont un groupe d'hydrates de carbone de faible poids moléculaire produits par l'hydrolyse de l'amidon ou du glycogène. Les dextrines sont des mélanges de polymères d'unités D-glucose liées par des liaisons glycosidiques -(1→4) ou -(1→6). |  |
| Amylodone : Amylodon est un genre éteint de chimères. Il se compose de quatre espèces décrites. A. karamysh est connu depuis le dernier Campanien ancien de Russie, le nom étant dérivé de la rivière Karamysh qui coule près de la localité type. A l'Eocène, deux espèces sont connues. A. venablesae et A. eocenica sont tous deux connus de l'argile de Londres d'âge yprésien d'Angleterre. Une plaque mandibulaire attribuée à l'origine à ce dernier a été trouvée dans le Bartonien des Barton Beds d'Angleterre, bien qu'elle ne corresponde à aucune espèce décrite. A. delheidi est connu de l'Argile de Boom d'âge Rupélien de Belgique. Toutes les espèces sont connues principalement par des mandibules isolées. Ils montrent une lente progression vers une capacité de cisaillement accrue. | |
| Phénobarbital : Le phénobarbital , également connu sous le nom de phénobarbital ou phénobarbe , ou sous le nom commercial Luminal , est un médicament du type barbiturique. Il est recommandé par l'Organisation mondiale de la santé (OMS) pour le traitement de certains types d'épilepsie dans les pays en développement. Dans le monde développé, il est couramment utilisé pour traiter les crises chez les jeunes enfants, tandis que d'autres médicaments sont généralement utilisés chez les enfants plus âgés et les adultes. Il peut être utilisé par voie intraveineuse, injecté dans un muscle ou pris par voie orale. La forme injectable peut être utilisée pour traiter l'état de mal épileptique. Le phénobarbital est parfois utilisé pour traiter les troubles du sommeil, l'anxiété et le sevrage médicamenteux et pour aider à la chirurgie. Il commence généralement à agir dans les cinq minutes lorsqu'il est utilisé par voie intraveineuse et une demi-heure lorsqu'il est administré par voie orale. Ses effets durent entre quatre heures et deux jours. |  |
| Amyloflagellule : Amyloflagellula est un genre de champignons de la famille des Marasmiaceae. | |
| Amylofonge : Amylofungus est un genre de champignons de la famille des Stéréacées. | |
| Amélogenèse : L'amélogenèse est la formation de l'émail sur les dents et commence lorsque la couronne se forme au cours du stade avancé en cloche du développement dentaire après que la dentinogénèse forme une première couche de dentine. La dentine doit être présente pour que l'émail se forme. Des améloblastes doivent également être présents pour que la dentinogenèse se poursuive. | |
| Amylase : Une amylase est une enzyme qui catalyse l'hydrolyse de l'amidon en sucres. L'amylase est présente dans la salive des humains et de certains autres mammifères, où elle commence le processus chimique de digestion. Les aliments qui contiennent de grandes quantités d'amidon mais peu de sucre, comme le riz et les pommes de terre, peuvent acquérir un goût légèrement sucré lorsqu'ils sont mâchés car l'amylase dégrade une partie de leur amidon en sucre. Le pancréas et la glande salivaire fabriquent de l'amylase pour hydrolyser l'amidon alimentaire en disaccharides et trisaccharides qui sont convertis par d'autres enzymes en glucose pour fournir de l'énergie au corps. Les plantes et certaines bactéries produisent également de l'amylase. Les protéines amylases spécifiques sont désignées par différentes lettres grecques. Toutes les amylases sont des glycoside hydrolases et agissent sur les liaisons α-1,4-glycosidiques. |  |
| Amylohyphe : Amylohyphus est un genre fongique de la famille des Stéréacées. Il a été circonscrit par le mycologue norvégien Leif Ryvarden en 1978 pour contenir le champignon à croûte unique Amylohyphus africanus . Le champignon, qui pousse sous forme de croûte mince sur le bois de feuillus, a une surface brun clair avec des bords lisses et jaunâtres. Les spores produites par le champignon sont cylindriques, à paroi mince et non amyloïdes, mesurant 12-15 par 5-7 7m. Amylohyphus africanus se trouve au Rwanda. | |
| Amyloïde : Les amyloïdes sont des agrégats de protéines caractérisés par une morphologie fibrillaire de 7 à 13 nm de diamètre, une structure secondaire en feuillets et une capacité à être colorés par des colorants particuliers, tels que le rouge Congo. Dans le corps humain, les amyloïdes ont été liés au développement de diverses maladies. Les amyloïdes pathogènes se forment lorsque des protéines auparavant saines perdent leur structure normale et leurs fonctions physiologiques (mauvais repliement) et forment des dépôts fibreux en plaques autour des cellules qui peuvent perturber le fonctionnement sain des tissus et des organes. |  |
| Bêta amyloïde : Le bêta-amyloïde désigne des peptides de 36 à 43 acides aminés qui sont le principal composant des plaques amyloïdes présentes dans le cerveau des personnes atteintes de la maladie d'Alzheimer. Les peptides dérivent de la protéine précurseur amyloïde (APP), qui est clivée par la bêta-sécrétase et la gamma-sécrétase pour donner Aβ. Les molécules Aβ peuvent s'agréger pour former des oligomères solubles flexibles qui peuvent exister sous plusieurs formes. On pense maintenant que certains oligomères mal repliés peuvent induire d'autres molécules Aβ à prendre également la forme oligomère mal repliée, conduisant à une réaction en chaîne semblable à une infection à prions. Les oligomères sont toxiques pour les cellules nerveuses. L'autre protéine impliquée dans la maladie d'Alzheimer, la protéine tau, forme également de tels oligomères mal repliés de type prion, et il existe des preuves qu'un Aβ mal replié peut induire un mauvais repliement de tau. | 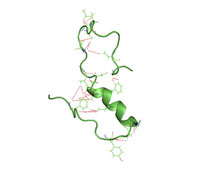 |
| Bêta amyloïde : Le bêta-amyloïde désigne des peptides de 36 à 43 acides aminés qui sont le principal composant des plaques amyloïdes présentes dans le cerveau des personnes atteintes de la maladie d'Alzheimer. Les peptides dérivent de la protéine précurseur amyloïde (APP), qui est clivée par la bêta-sécrétase et la gamma-sécrétase pour donner Aβ. Les molécules Aβ peuvent s'agréger pour former des oligomères solubles flexibles qui peuvent exister sous plusieurs formes. On pense maintenant que certains oligomères mal repliés peuvent induire d'autres molécules Aβ à prendre également la forme oligomère mal repliée, conduisant à une réaction en chaîne semblable à une infection à prions. Les oligomères sont toxiques pour les cellules nerveuses. L'autre protéine impliquée dans la maladie d'Alzheimer, la protéine tau, forme également de tels oligomères mal repliés de type prion, et il existe des preuves qu'un Aβ mal replié peut induire un mauvais repliement de tau. |  |
| Bêta amyloïde : Le bêta-amyloïde désigne des peptides de 36 à 43 acides aminés qui sont le principal composant des plaques amyloïdes présentes dans le cerveau des personnes atteintes de la maladie d'Alzheimer. Les peptides dérivent de la protéine précurseur amyloïde (APP), qui est clivée par la bêta-sécrétase et la gamma-sécrétase pour donner Aβ. Les molécules Aβ peuvent s'agréger pour former des oligomères solubles flexibles qui peuvent exister sous plusieurs formes. On pense maintenant que certains oligomères mal repliés peuvent induire d'autres molécules Aβ à prendre également la forme oligomère mal repliée, conduisant à une réaction en chaîne semblable à une infection à prions. Les oligomères sont toxiques pour les cellules nerveuses. L'autre protéine impliquée dans la maladie d'Alzheimer, la protéine tau, forme également de tels oligomères mal repliés de type prion, et il existe des preuves qu'un Aβ mal replié peut induire un mauvais repliement de tau. |  |
| Protéine précurseur bêta-amyloïde : La protéine précurseur bêta-amyloïde ( APP ) est une protéine membranaire intégrale exprimée dans de nombreux tissus et concentrée dans les synapses des neurones. Il fonctionne comme un récepteur de surface cellulaire et a été impliqué en tant que régulateur de la formation des synapses, de la plasticité neurale, de l'activité antimicrobienne et de l'exportation du fer. Il est codé par le gène APP et est surtout connu comme la molécule précurseur dont la protéolyse génère le bêta-amyloïde (Aβ), un polypeptide contenant 37 à 49 résidus d'acides aminés, dont la forme fibrillaire amyloïde est le principal composant des plaques amyloïdes trouvées dans le cerveau. des patients atteints de la maladie d'Alzheimer. |  |
| Sécrétase de la protéine précurseur bêta-amyloïde : Les sécrétases sont des enzymes qui "coupent" des morceaux d'une protéine plus longue qui est incrustée dans la membrane cellulaire. |  |
| Anomalies d'imagerie liées à l'amyloïde : Les anomalies d'imagerie liées à l'amyloïde ( ARIA ) sont des différences anormales observées dans la neuroimagerie des patients atteints de la maladie d'Alzheimer, associées aux thérapies modifiant l'amyloïde, en particulier les anticorps monoclonaux humains tels que l'aducanumab. Il existe deux types d'ARIA - ARIA-E et ARIA-H. Le phénomène a été observé pour la première fois dans les essais sur le bapineuzumab. |  |
| Bêta amyloïde : Le bêta-amyloïde désigne des peptides de 36 à 43 acides aminés qui sont le principal composant des plaques amyloïdes présentes dans le cerveau des personnes atteintes de la maladie d'Alzheimer. Les peptides dérivent de la protéine précurseur amyloïde (APP), qui est clivée par la bêta-sécrétase et la gamma-sécrétase pour donner Aβ. Les molécules Aβ peuvent s'agréger pour former des oligomères solubles flexibles qui peuvent exister sous plusieurs formes. On pense maintenant que certains oligomères mal repliés peuvent induire d'autres molécules Aβ à prendre également la forme oligomère mal repliée, conduisant à une réaction en chaîne semblable à une infection à prions. Les oligomères sont toxiques pour les cellules nerveuses. L'autre protéine impliquée dans la maladie d'Alzheimer, la protéine tau, forme également de tels oligomères mal repliés de type prion, et il existe des preuves qu'un Aβ mal replié peut induire un mauvais repliement de tau. |  |
| Amyloïde (journal) : Amyloïde : le Journal of Protein Folding Disorders est une revue scientifique à comité de lecture qui publie des articles de recherche et de synthèse originaux sur tous les aspects des groupes de protéines et des troubles associés classés comme amyloses ainsi que d'autres troubles associés à un repliement anormal des protéines. Le Journal se concentre principalement sur l'étiologie, la pathogenèse, l'histopathologie, la structure chimique et la nature de la fibrillogenèse et publie également des articles sur les aspects génétiques de bon nombre de ces troubles. C'est le journal officiel de la Société internationale d'amylose . Le Journal a été créé en 1994 sous le nom « AMYLOID : The International Journal of Experimental & Clinical Investigation » jusqu'au changement de nom en 2004. Le facteur d'impact en 2017 était de 4,048. Le Dr Alan Cohen a été le rédacteur en chef fondateur et, de 1994 à 2010, le premier rédacteur en chef d' Amyloid: The Journal of Protein Folding Disorders . Le rédacteur en chef actuel est Per Westermark. | |
| Amyloïde (journal) : Amyloïde : le Journal of Protein Folding Disorders est une revue scientifique à comité de lecture qui publie des articles de recherche et de synthèse originaux sur tous les aspects des groupes de protéines et des troubles associés classés comme amyloses ainsi que d'autres troubles associés à un repliement anormal des protéines. Le Journal se concentre principalement sur l'étiologie, la pathogenèse, l'histopathologie, la structure chimique et la nature de la fibrillogenèse et publie également des articles sur les aspects génétiques de bon nombre de ces troubles. C'est le journal officiel de la Société internationale d'amylose . Le Journal a été créé en 1994 sous le nom « AMYLOID : The International Journal of Experimental & Clinical Investigation » jusqu'au changement de nom en 2004. Le facteur d'impact en 2017 était de 4,048. Le Dr Alan Cohen a été le rédacteur en chef fondateur et, de 1994 à 2010, le premier rédacteur en chef d' Amyloid: The Journal of Protein Folding Disorders . Le rédacteur en chef actuel est Per Westermark. | |
| Amyloïde (homonymie) : Un amyloïde est l'un quelconque de certains agrégats de protéines fibreuses insolubles. | |
| Amyloïde (journal) : Amyloïde : le Journal of Protein Folding Disorders est une revue scientifique à comité de lecture qui publie des articles de recherche et de synthèse originaux sur tous les aspects des groupes de protéines et des troubles associés classés comme amyloses ainsi que d'autres troubles associés à un repliement anormal des protéines. Le Journal se concentre principalement sur l'étiologie, la pathogenèse, l'histopathologie, la structure chimique et la nature de la fibrillogenèse et publie également des articles sur les aspects génétiques de bon nombre de ces troubles. C'est le journal officiel de la Société internationale d'amylose . Le Journal a été créé en 1994 sous le nom « AMYLOID : The International Journal of Experimental & Clinical Investigation » jusqu'au changement de nom en 2004. Le facteur d'impact en 2017 était de 4,048. Le Dr Alan Cohen a été le rédacteur en chef fondateur et, de 1994 à 2010, le premier rédacteur en chef d' Amyloid: The Journal of Protein Folding Disorders . Le rédacteur en chef actuel est Per Westermark. | |
| Amyloïde (mycologie): En mycologie, un tissu ou une caractéristique est dit amyloïde s'il présente une réaction amyloïde positive lorsqu'il est soumis à un test chimique brut utilisant de l'iode comme ingrédient du réactif de Melzer ou de la solution de Lugol, produisant une coloration bleue à bleu-noir. Le terme « amyloïde » est dérivé du latin amyloideus (« semblable à l'amidon »). Il fait référence au fait que l'amidon donne une réaction similaire, également appelée réaction amyloïde. Le test peut porter sur des caractéristiques microscopiques, telles que les parois des spores ou des hyphes, ou l'appareil apical ou la paroi entière de l'asque d'un asque, ou être une réaction macroscopique sur un tissu où une goutte de réactif est appliquée. Les réactions négatives, appelées inamyloïdes ou non amyloïdes , concernent les structures qui restent jaune-brun pâle ou claires. Une réaction produisant une coloration rougeâtre foncé à brun rougeâtre est appelée réaction dextrinoïde ou réaction hémiamyloïde . | |
| Amyloïde sérique A : Les protéines sériques amyloïdes A (SAA) sont une famille d'apolipoprotéines associées aux lipoprotéines de haute densité (HDL) dans le plasma. Différentes isoformes de SAA sont exprimées de manière constitutive à différents niveaux ou en réponse à des stimuli inflammatoires. Ces protéines sont produites principalement par le foie. | |
| Bêta amyloïde : Le bêta-amyloïde désigne des peptides de 36 à 43 acides aminés qui sont le principal composant des plaques amyloïdes présentes dans le cerveau des personnes atteintes de la maladie d'Alzheimer. Les peptides dérivent de la protéine précurseur amyloïde (APP), qui est clivée par la bêta-sécrétase et la gamma-sécrétase pour donner Aβ. Les molécules Aβ peuvent s'agréger pour former des oligomères solubles flexibles qui peuvent exister sous plusieurs formes. On pense maintenant que certains oligomères mal repliés peuvent induire d'autres molécules Aβ à prendre également la forme oligomère mal repliée, conduisant à une réaction en chaîne semblable à une infection à prions. Les oligomères sont toxiques pour les cellules nerveuses. L'autre protéine impliquée dans la maladie d'Alzheimer, la protéine tau, forme également de tels oligomères mal repliés de type prion, et il existe des preuves qu'un Aβ mal replié peut induire un mauvais repliement de tau. |  |
| Neuropathie amyloïde familiale : Les neuropathies amyloïdes familiales sont un groupe rare de maladies autosomiques dominantes dans lesquelles le système nerveux autonome et/ou d'autres nerfs sont compromis par l'agrégation de protéines et/ou la formation de fibrilles amyloïdes. | |
| Composant amyloïde P sérique : Le composant amyloïde P sérique (SAP) est la forme sérique identique du composant amyloïde P (AP), une protéine pentamérique de 25 kDa identifiée pour la première fois comme le constituant pentagonal des dépôts pathologiques in vivo appelés « amyloïde ». APCS est son gène humain. |  |
| Amyline : L'amyline, ou polypeptide amyloïde des îlots ( IAPP ), est une hormone peptidique à 37 résidus. Il est cosécrété avec l'insuline des cellules β pancréatiques dans un rapport d'environ 100:1 (insuline:amyline). L'amyline joue un rôle dans la régulation glycémique en ralentissant la vidange gastrique et en favorisant la satiété, empêchant ainsi les pics post-prandiaux de la glycémie. |  |
| Angiopathie amyloïde cérébrale : L'angiopathie amyloïde cérébrale (AAC) est une forme d'angiopathie dans laquelle le peptide bêta-amyloïde se dépose dans les parois des vaisseaux sanguins petits à moyens du système nerveux central et des méninges. Le terme congophile est parfois utilisé car la présence d'agrégats anormaux d'amyloïde peut être mise en évidence par un examen microscopique du tissu cérébral après coloration au rouge Congo. La matière amyloïde ne se trouve que dans le cerveau et, en tant que telle, la maladie n'est pas liée à d'autres formes d'amylose. |  |
| Amylose AA : L'amylose AA est une forme d'amylose, une maladie caractérisée par le dépôt anormal de fibres de protéines insolubles dans l'espace extracellulaire de divers tissus et organes. Dans l'amylose AA, la protéine déposée est la protéine amyloïde A sérique (SAA), une protéine de phase aiguë qui est normalement soluble et dont la concentration plasmatique est la plus élevée pendant l'inflammation. | |
| Bêta amyloïde : Le bêta-amyloïde désigne des peptides de 36 à 43 acides aminés qui sont le principal composant des plaques amyloïdes présentes dans le cerveau des personnes atteintes de la maladie d'Alzheimer. Les peptides dérivent de la protéine précurseur amyloïde (APP), qui est clivée par la bêta-sécrétase et la gamma-sécrétase pour donner Aβ. Les molécules Aβ peuvent s'agréger pour former des oligomères solubles flexibles qui peuvent exister sous plusieurs formes. On pense maintenant que certains oligomères mal repliés peuvent induire d'autres molécules Aβ à prendre également la forme oligomère mal repliée, conduisant à une réaction en chaîne semblable à une infection à prions. Les oligomères sont toxiques pour les cellules nerveuses. L'autre protéine impliquée dans la maladie d'Alzheimer, la protéine tau, forme également de tels oligomères mal repliés de type prion, et il existe des preuves qu'un Aβ mal replié peut induire un mauvais repliement de tau. |  |
| Bêta amyloïde : Le bêta-amyloïde désigne des peptides de 36 à 43 acides aminés qui sont le principal composant des plaques amyloïdes présentes dans le cerveau des personnes atteintes de la maladie d'Alzheimer. Les peptides dérivent de la protéine précurseur amyloïde (APP), qui est clivée par la bêta-sécrétase et la gamma-sécrétase pour donner Aβ. Les molécules Aβ peuvent s'agréger pour former des oligomères solubles flexibles qui peuvent exister sous plusieurs formes. On pense maintenant que certains oligomères mal repliés peuvent induire d'autres molécules Aβ à prendre également la forme oligomère mal repliée, conduisant à une réaction en chaîne semblable à une infection à prions. Les oligomères sont toxiques pour les cellules nerveuses. L'autre protéine impliquée dans la maladie d'Alzheimer, la protéine tau, forme également de tels oligomères mal repliés de type prion, et il existe des preuves qu'un Aβ mal replié peut induire un mauvais repliement de tau. |  |
| Protéine précurseur bêta-amyloïde : La protéine précurseur bêta-amyloïde ( APP ) est une protéine membranaire intégrale exprimée dans de nombreux tissus et concentrée dans les synapses des neurones. Il fonctionne comme un récepteur de surface cellulaire et a été impliqué en tant que régulateur de la formation des synapses, de la plasticité neurale, de l'activité antimicrobienne et de l'exportation du fer. Il est codé par le gène APP et est surtout connu comme la molécule précurseur dont la protéolyse génère le bêta-amyloïde (Aβ), un polypeptide contenant 37 à 49 résidus d'acides aminés, dont la forme fibrillaire amyloïde est le principal composant des plaques amyloïdes trouvées dans le cerveau. des patients atteints de la maladie d'Alzheimer. |  |
| Bêta amyloïde : Le bêta-amyloïde désigne des peptides de 36 à 43 acides aminés qui sont le principal composant des plaques amyloïdes présentes dans le cerveau des personnes atteintes de la maladie d'Alzheimer. Les peptides dérivent de la protéine précurseur amyloïde (APP), qui est clivée par la bêta-sécrétase et la gamma-sécrétase pour donner Aβ. Les molécules Aβ peuvent s'agréger pour former des oligomères solubles flexibles qui peuvent exister sous plusieurs formes. On pense maintenant que certains oligomères mal repliés peuvent induire d'autres molécules Aβ à prendre également la forme oligomère mal repliée, conduisant à une réaction en chaîne semblable à une infection à prions. Les oligomères sont toxiques pour les cellules nerveuses. L'autre protéine impliquée dans la maladie d'Alzheimer, la protéine tau, forme également de tels oligomères mal repliés de type prion, et il existe des preuves qu'un Aβ mal replié peut induire un mauvais repliement de tau. |  |
| Bêta amyloïde : Le bêta-amyloïde désigne des peptides de 36 à 43 acides aminés qui sont le principal composant des plaques amyloïdes présentes dans le cerveau des personnes atteintes de la maladie d'Alzheimer. Les peptides dérivent de la protéine précurseur amyloïde (APP), qui est clivée par la bêta-sécrétase et la gamma-sécrétase pour donner Aβ. Les molécules Aβ peuvent s'agréger pour former des oligomères solubles flexibles qui peuvent exister sous plusieurs formes. On pense maintenant que certains oligomères mal repliés peuvent induire d'autres molécules Aβ à prendre également la forme oligomère mal repliée, conduisant à une réaction en chaîne semblable à une infection à prions. Les oligomères sont toxiques pour les cellules nerveuses. L'autre protéine impliquée dans la maladie d'Alzheimer, la protéine tau, forme également de tels oligomères mal repliés de type prion, et il existe des preuves qu'un Aβ mal replié peut induire un mauvais repliement de tau. |  |
| Amyloïde : Les amyloïdes sont des agrégats de protéines caractérisés par une morphologie fibrillaire de 7 à 13 nm de diamètre, une structure secondaire en feuillets et une capacité à être colorés par des colorants particuliers, tels que le rouge Congo. Dans le corps humain, les amyloïdes ont été liés au développement de diverses maladies. Les amyloïdes pathogènes se forment lorsque des protéines auparavant saines perdent leur structure normale et leurs fonctions physiologiques (mauvais repliement) et forment des dépôts fibreux en plaques autour des cellules qui peuvent perturber le fonctionnement sain des tissus et des organes. |  |
| Cardiomyopathie amyloïde : La cardiomyopathie amyloïde est une affection entraînant la mort d'une partie du myocarde. Elle est associée à la production et à la libération systémiques de nombreuses protéines amyloïdogènes, en particulier la chaîne légère des immunoglobulines ou la transthyrétine (TTR). Elle peut être caractérisée par le dépôt extracellulaire d'amyloïdes, des protéines pliables qui se collent pour former des fibrilles dans le cœur. L'amyloïde peut être vu sous lumière polarisée dans la biopsie colorée en rouge Congo. | |
| Amyloïde : Les amyloïdes sont des agrégats de protéines caractérisés par une morphologie fibrillaire de 7 à 13 nm de diamètre, une structure secondaire en feuillets et une capacité à être colorés par des colorants particuliers, tels que le rouge Congo. Dans le corps humain, les amyloïdes ont été liés au développement de diverses maladies. Les amyloïdes pathogènes se forment lorsque des protéines auparavant saines perdent leur structure normale et leurs fonctions physiologiques (mauvais repliement) et forment des dépôts fibreux en plaques autour des cellules qui peuvent perturber le fonctionnement sain des tissus et des organes. |  |
| Amyloïde : Les amyloïdes sont des agrégats de protéines caractérisés par une morphologie fibrillaire de 7 à 13 nm de diamètre, une structure secondaire en feuillets et une capacité à être colorés par des colorants particuliers, tels que le rouge Congo. Dans le corps humain, les amyloïdes ont été liés au développement de diverses maladies. Les amyloïdes pathogènes se forment lorsque des protéines auparavant saines perdent leur structure normale et leurs fonctions physiologiques (mauvais repliement) et forment des dépôts fibreux en plaques autour des cellules qui peuvent perturber le fonctionnement sain des tissus et des organes. |  |
| Amylose : L'amylose est un groupe de maladies dans lesquelles des protéines anormales, appelées fibrilles amyloïdes, s'accumulent dans les tissus. Il existe plusieurs types avec des symptômes variables; les signes et symptômes peuvent inclure diarrhée, perte de poids, sensation de fatigue, hypertrophie de la langue, saignement, engourdissement, sensation de faiblesse en se tenant debout, gonflement des jambes ou hypertrophie de la rate. | 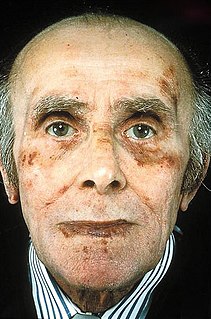 |
| Amyloïde : Les amyloïdes sont des agrégats de protéines caractérisés par une morphologie fibrillaire de 7 à 13 nm de diamètre, une structure secondaire en feuillets et une capacité à être colorés par des colorants particuliers, tels que le rouge Congo. Dans le corps humain, les amyloïdes ont été liés au développement de diverses maladies. Les amyloïdes pathogènes se forment lorsque des protéines auparavant saines perdent leur structure normale et leurs fonctions physiologiques (mauvais repliement) et forment des dépôts fibreux en plaques autour des cellules qui peuvent perturber le fonctionnement sain des tissus et des organes. |  |
| Amyloïde : Les amyloïdes sont des agrégats de protéines caractérisés par une morphologie fibrillaire de 7 à 13 nm de diamètre, une structure secondaire en feuillets et une capacité à être colorés par des colorants particuliers, tels que le rouge Congo. Dans le corps humain, les amyloïdes ont été liés au développement de diverses maladies. Les amyloïdes pathogènes se forment lorsque des protéines auparavant saines perdent leur structure normale et leurs fonctions physiologiques (mauvais repliement) et forment des dépôts fibreux en plaques autour des cellules qui peuvent perturber le fonctionnement sain des tissus et des organes. |  |
| Amyloïde : Les amyloïdes sont des agrégats de protéines caractérisés par une morphologie fibrillaire de 7 à 13 nm de diamètre, une structure secondaire en feuillets et une capacité à être colorés par des colorants particuliers, tels que le rouge Congo. Dans le corps humain, les amyloïdes ont été liés au développement de diverses maladies. Les amyloïdes pathogènes se forment lorsque des protéines auparavant saines perdent leur structure normale et leurs fonctions physiologiques (mauvais repliement) et forment des dépôts fibreux en plaques autour des cellules qui peuvent perturber le fonctionnement sain des tissus et des organes. |  |
| Amyloïde : Les amyloïdes sont des agrégats de protéines caractérisés par une morphologie fibrillaire de 7 à 13 nm de diamètre, une structure secondaire en feuillets et une capacité à être colorés par des colorants particuliers, tels que le rouge Congo. Dans le corps humain, les amyloïdes ont été liés au développement de diverses maladies. Les amyloïdes pathogènes se forment lorsque des protéines auparavant saines perdent leur structure normale et leurs fonctions physiologiques (mauvais repliement) et forment des dépôts fibreux en plaques autour des cellules qui peuvent perturber le fonctionnement sain des tissus et des organes. |  |
| Biochimie de la maladie d'Alzheimer : La biochimie de la maladie d'Alzheimer , la cause la plus fréquente de démence, n'est pas encore très bien comprise. La maladie d'Alzheimer (MA) a été identifiée comme une protéopathie, une maladie du mauvais repliement des protéines due à l'accumulation de protéine bêta-amyloïde (Aβ) anormalement repliée dans le cerveau. La bêta-amyloïde est un peptide court qui est un sous-produit protéolytique anormal de la protéine précurseur bêta-amyloïde (APP) de la protéine transmembranaire, dont la fonction n'est pas claire mais qui serait impliquée dans le développement neuronal. Les présénilines sont des composants du complexe protéolytique impliqué dans le traitement et la dégradation de l'APP. | |
| Amylose AL : L' amylose à chaînes légères amyloïdes ( AL ), également connue sous le nom d'amylose primaire , est la forme la plus courante d'amylose systémique aux États-Unis. La maladie est causée lorsque les cellules productrices d'anticorps d'une personne ne fonctionnent pas correctement et produisent des fibres protéiques anormales constituées de composants d'anticorps appelés chaînes légères. Ces chaînes légères se rassemblent pour former des dépôts amyloïdes qui peuvent causer de graves dommages à différents organes. Les chaînes légères anormales dans l'urine sont parfois appelées "protéines de Bence Jones". | |
| Amylose rénale familiale : L'amylose rénale familiale est une forme d'amylose se présentant principalement dans le rein. |  |
| Amyloïde : Les amyloïdes sont des agrégats de protéines caractérisés par une morphologie fibrillaire de 7 à 13 nm de diamètre, une structure secondaire en feuillets et une capacité à être colorés par des colorants particuliers, tels que le rouge Congo. Dans le corps humain, les amyloïdes ont été liés au développement de diverses maladies. Les amyloïdes pathogènes se forment lorsque des protéines auparavant saines perdent leur structure normale et leurs fonctions physiologiques (mauvais repliement) et forment des dépôts fibreux en plaques autour des cellules qui peuvent perturber le fonctionnement sain des tissus et des organes. |  |
| Neuropathie amyloïde familiale : Les neuropathies amyloïdes familiales sont un groupe rare de maladies autosomiques dominantes dans lesquelles le système nerveux autonome et/ou d'autres nerfs sont compromis par l'agrégation de protéines et/ou la formation de fibrilles amyloïdes. | |
| Amyloïde : Les amyloïdes sont des agrégats de protéines caractérisés par une morphologie fibrillaire de 7 à 13 nm de diamètre, une structure secondaire en feuillets et une capacité à être colorés par des colorants particuliers, tels que le rouge Congo. Dans le corps humain, les amyloïdes ont été liés au développement de diverses maladies. Les amyloïdes pathogènes se forment lorsque des protéines auparavant saines perdent leur structure normale et leurs fonctions physiologiques (mauvais repliement) et forment des dépôts fibreux en plaques autour des cellules qui peuvent perturber le fonctionnement sain des tissus et des organes. |  |
| Plaques amyloïdes : Les plaques amyloïdes sont des dépôts extracellulaires de la protéine bêta-amyloïde (Aβ) principalement dans la matière grise du cerveau. Des éléments neuronaux dégénératifs et une abondance de microglies et d'astrocytes peuvent être associés aux plaques amyloïdes. Certaines plaques apparaissent dans le cerveau à la suite de la sénescence (vieillissement), mais un grand nombre de plaques et d'enchevêtrements neurofibrillaires sont des caractéristiques de la maladie d'Alzheimer. Les neurites anormaux dans les plaques amyloïdes sont des axones et des dendrites tortueux et souvent enflés. Les neurites contiennent une variété d'organites et de débris cellulaires, et beaucoup d'entre eux comprennent des filaments hélicoïdaux appariés caractéristiques, la composante ultrastructurale des enchevêtrements neurofibrillaires. Les plaques sont de forme et de taille très variables; dans les coupes de tissus immunocolorées pour Aβ, elles comprennent une courbe de distribution de taille log-normale avec une surface moyenne de plaque de 400 à 450 micromètres carrés (µm²). Les plus petites plaques, qui sont souvent constituées de dépôts diffus d'Aβ, sont particulièrement nombreuses. La taille apparente des plaques est influencée par le type de colorant utilisé pour les détecter et par le plan à travers lequel elles sont sectionnées pour être analysées au microscope. Des plaques se forment lorsque Aβ se replie mal et s'agrège en oligomères et polymères plus longs, ces derniers étant caractéristiques de l'amyloïde. On pense que l'A mal replié et agrégé est neurotoxique, en particulier dans son état oligomérique. |  |
| Plaques amyloïdes : Les plaques amyloïdes sont des dépôts extracellulaires de la protéine bêta-amyloïde (Aβ) principalement dans la matière grise du cerveau. Des éléments neuronaux dégénératifs et une abondance de microglies et d'astrocytes peuvent être associés aux plaques amyloïdes. Certaines plaques apparaissent dans le cerveau à la suite de la sénescence (vieillissement), mais un grand nombre de plaques et d'enchevêtrements neurofibrillaires sont des caractéristiques de la maladie d'Alzheimer. Les neurites anormaux dans les plaques amyloïdes sont des axones et des dendrites tortueux et souvent enflés. Les neurites contiennent une variété d'organites et de débris cellulaires, et beaucoup d'entre eux comprennent des filaments hélicoïdaux appariés caractéristiques, la composante ultrastructurale des enchevêtrements neurofibrillaires. Les plaques sont de forme et de taille très variables; dans les coupes de tissus immunocolorées pour Aβ, elles comprennent une courbe de distribution de taille log-normale avec une surface moyenne de plaque de 400 à 450 micromètres carrés (µm²). Les plus petites plaques, qui sont souvent constituées de dépôts diffus d'Aβ, sont particulièrement nombreuses. La taille apparente des plaques est influencée par le type de colorant utilisé pour les détecter et par le plan à travers lequel elles sont sectionnées pour être analysées au microscope. Des plaques se forment lorsque Aβ se replie mal et s'agrège en oligomères et polymères plus longs, ces derniers étant caractéristiques de l'amyloïde. On pense que l'A mal replié et agrégé est neurotoxique, en particulier dans son état oligomérique. |  |
| Neuropathie amyloïde familiale : Les neuropathies amyloïdes familiales sont un groupe rare de maladies autosomiques dominantes dans lesquelles le système nerveux autonome et/ou d'autres nerfs sont compromis par l'agrégation de protéines et/ou la formation de fibrilles amyloïdes. | |
| Protéine précurseur bêta-amyloïde : La protéine précurseur bêta-amyloïde ( APP ) est une protéine membranaire intégrale exprimée dans de nombreux tissus et concentrée dans les synapses des neurones. Il fonctionne comme un récepteur de surface cellulaire et a été impliqué en tant que régulateur de la formation des synapses, de la plasticité neurale, de l'activité antimicrobienne et de l'exportation du fer. Il est codé par le gène APP et est surtout connu comme la molécule précurseur dont la protéolyse génère le bêta-amyloïde (Aβ), un polypeptide contenant 37 à 49 résidus d'acides aminés, dont la forme fibrillaire amyloïde est le principal composant des plaques amyloïdes trouvées dans le cerveau. des patients atteints de la maladie d'Alzheimer. |  |
| Sécrétase de la protéine précurseur bêta-amyloïde : Les sécrétases sont des enzymes qui "coupent" des morceaux d'une protéine plus longue qui est incrustée dans la membrane cellulaire. |  |
| Amyloïde : Les amyloïdes sont des agrégats de protéines caractérisés par une morphologie fibrillaire de 7 à 13 nm de diamètre, une structure secondaire en feuillets et une capacité à être colorés par des colorants particuliers, tels que le rouge Congo. Dans le corps humain, les amyloïdes ont été liés au développement de diverses maladies. Les amyloïdes pathogènes se forment lorsque des protéines auparavant saines perdent leur structure normale et leurs fonctions physiologiques (mauvais repliement) et forment des dépôts fibreux en plaques autour des cellules qui peuvent perturber le fonctionnement sain des tissus et des organes. |  |
| Amyloïde : Les amyloïdes sont des agrégats de protéines caractérisés par une morphologie fibrillaire de 7 à 13 nm de diamètre, une structure secondaire en feuillets et une capacité à être colorés par des colorants particuliers, tels que le rouge Congo. Dans le corps humain, les amyloïdes ont été liés au développement de diverses maladies. Les amyloïdes pathogènes se forment lorsque des protéines auparavant saines perdent leur structure normale et leurs fonctions physiologiques (mauvais repliement) et forment des dépôts fibreux en plaques autour des cellules qui peuvent perturber le fonctionnement sain des tissus et des organes. |  |
| Purpura amyloïde : Le purpura amyloïde est une affection caractérisée par des saignements sous la peau (purpura) chez certaines personnes atteintes d'amylose. Sa cause est inconnue, mais on pense que les défauts de coagulation causés par l'amyloïde y contribuent. |  |
| Amyloïde (mycologie): En mycologie, un tissu ou une caractéristique est dit amyloïde s'il présente une réaction amyloïde positive lorsqu'il est soumis à un test chimique brut utilisant de l'iode comme ingrédient du réactif de Melzer ou de la solution de Lugol, produisant une coloration bleue à bleu-noir. Le terme « amyloïde » est dérivé du latin amyloideus (« semblable à l'amidon »). Il fait référence au fait que l'amidon donne une réaction similaire, également appelée réaction amyloïde. Le test peut porter sur des caractéristiques microscopiques, telles que les parois des spores ou des hyphes, ou l'appareil apical ou la paroi entière de l'asque d'un asque, ou être une réaction macroscopique sur un tissu où une goutte de réactif est appliquée. Les réactions négatives, appelées inamyloïdes ou non amyloïdes , concernent les structures qui restent jaune-brun pâle ou claires. Une réaction produisant une coloration rougeâtre foncé à brun rougeâtre est appelée réaction dextrinoïde ou réaction hémiamyloïde . | |
| Porpoloma umbrosum : Porpoloma umbrosum , communément appelé tricholome amyloïde , est une espèce de champignon de la famille des Tricholomataceae et l'espèce type du genre Porpoloma . Il a été décrit pour la première fois scientifiquement par les mycologues Alexander H. Smith et Maurice B. Walters en 1943 comme une espèce de Tricholoma . Rolf Singer l'a transféré à Porpoloma en 1962. Le champignon se trouve en Amérique du Nord, où il fructifie seul ou en petits groupes sous les conifères. Bien qu'il ressemble à l'espèce Tricholoma , il se distingue de ce genre par ses spores amyloïdes. |  |
Rechercher dans ce blog
dimanche 6 juin 2021
2-Heptanone, Amyl nitrate, Amyl nitrate
Inscription à :
Publier les commentaires (Atom)
-
Antanartia délius : Antanartia delius , l' amiral des forêts ou amiral orange , est un papillon de la famille des Nymphalidae. ...
-
Akim Swedru (circonscription parlementaire du Ghana): Akim Swedru est l'une des circonscriptions représentées au Parlement du Ghan...
-
Rallye d'Akademos: L' Akademos Rally est un rallye automobile annuel organisé à Victoria, en Australie, par le Melbourne Unive...
Aucun commentaire:
Enregistrer un commentaire